nur für Forschungszwecke
SR1001 ROR Agonist
Kat.-Nr.S6724
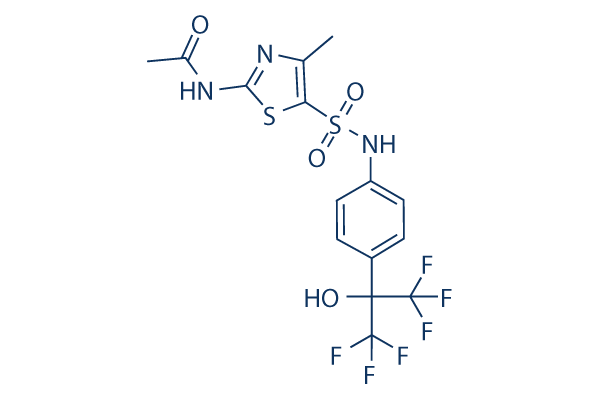
Chemische Struktur
Molekulargewicht: 477.40
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Weitere ROR Inhibitoren | SR1078 GSK2981278 Cintirorgon (LYC-55716) Neoruscogenin SR3335 TMP778 Cedirogant S18-000003 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 477.40 | Formel | C15H13F6N3O4S2 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 1335106-03-0 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(SC(=N1)NC(=O)C)S(=O)(=O)NC2=CC=C(C=C2)C(C(F)(F)F)(C(F)(F)F)O | ||
Löslichkeit
|
In vitro |
DMSO
: 95 mg/mL
(198.99 mM)
Ethanol : 95 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
RORγ
111 nM(Ki)
RORα
172 nM(Ki)
|
|---|---|
| In vitro |
SR1001 bindet spezifisch an die Ligandenbindungsdomänen (LBDs) von RORα und RORγt, was eine Konformationsänderung innerhalb des LBD hervorruft, die eine Neupositionierung der Helix 12 umfasst, was zu einer verminderten Affinität für Coaktivatoren und einer erhöhten Affinität für Korepressoren führt, was die transkriptionelle Aktivität der Rezeptoren unterdrückt. |
| In vivo |
SR1001 unterdrückt die Immunantwort, einschließlich TH17-Zellen in vitro und in vivo, TH1-Zellen in vivo, die Autoantikörperproduktion, erhält den Insulinspiegel aufrecht und erhöht die Foxp3-Expression. Diese Verbindung schützt wirksam vor pathologischer Neovaskularisation sowohl bei sauerstoffinduzierter Retinopathie als auch bei einem anderen angiogenen Modell von Mäusen mit sehr niedrigdichtem Lipoproteinrezeptor (Vldlr)-Mangel (Vldlr −/−) mit spontaner subretinaler Neovaskularisation. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
