nur für Forschungszwecke
Tenofovir hydrate Reverse Transcriptase Inhibitor
Kat.-Nr.S4879
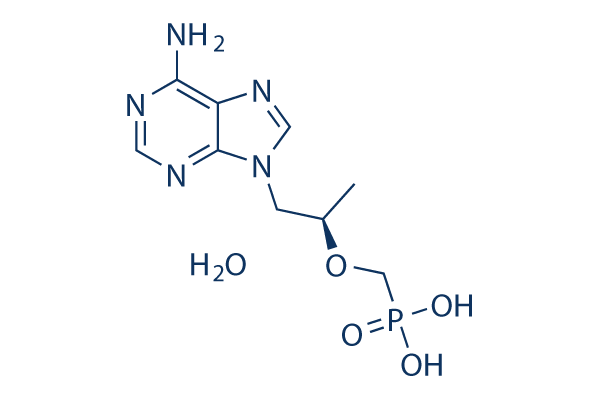
Chemische Struktur
Molekulargewicht: 305.23
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite HIV HCV Protease |
|---|---|
| Weitere Reverse Transcriptase Inhibitoren | Dapivirine (TMC120) Fangchinoline Salicylanilide 3'-Fluoro-3'-deoxythymidine (Alovudine) Ulonivirine Lersivirine (UK-453061) Bifendate 4-Chloro-2-(trifluoroacetyl)aniline hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 305.23 | Formel | C9H16N5O5P |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 206184-49-8 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | GS-1278 hydrate | Smiles | O.CC(C[N]1C=NC2=C(N)N=CN=C12)OC[P](O)(O)=O | ||
Löslichkeit
|
In vitro |
Water : 10 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Tenofovir reduziert den viralen zytopathischen Effekt von HIV-1(IIIB), HIV-2(ROD) und HIV(EHO) mit EC50 von 1,15 μg/mL, 1,12 μg/mL und 1,05 μg/mL in MT-4-Zellen. Tenofovir reduziert auch den viralen zytopathischen Effekt von SIV(mac251), SIV(B670), SHIV(89.6) und SHIV(RTSHIV). Tenofovir ist einzigartig aktiv gegen multinukleosidresistentes HIV, das die Q151M-Mutation exprimiert, zeigt aber eine reduzierte Anfälligkeit für die T69S-Insertionsmutationen. Tenofovir hemmt die Aktivität des Hepatitis-B-Virus (HBV) in HepG2 2.2.15-, HepAD38- und HepAD79-Zellen. Tenofovir (4 μM) hemmt vollständig das Wachstum von HIVIIIB in MT-2-Zellen. Tenofovir hemmt die Synthese von Negativstrang-Strong-Stop-DNA mit IC50 von 9 µM für Wildtyp-RT, 6 µM für M184V RT und 50 µM für K65R RT. |
|---|---|
| In vivo |
Tenofovir (30 mg/kg) verhindert vollständig eine SIV-Infektion bei allen Makaken ohne Toxizität. Die Tenofovir-Behandlung reduziert die Plasmaspiegel der viralen RNA auf nicht nachweisbare Werte, mit parallelen Abnahmen der Infektiosität von Plasma und infektiösen Zellen in peripheren mononukleären Blutzellen und Liquor (CSF) sowie einer Stabilisierung der CD4+-T-Zellzahlen. Tenofovir (30 mg/kg, s.c.) hebt die HIV-Infektion über intravaginale Exposition bei Schweinsaffen vollständig auf. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
