nur für Forschungszwecke
Zofenopril calcium RAAS Hemmer
Kat.-Nr.S5712
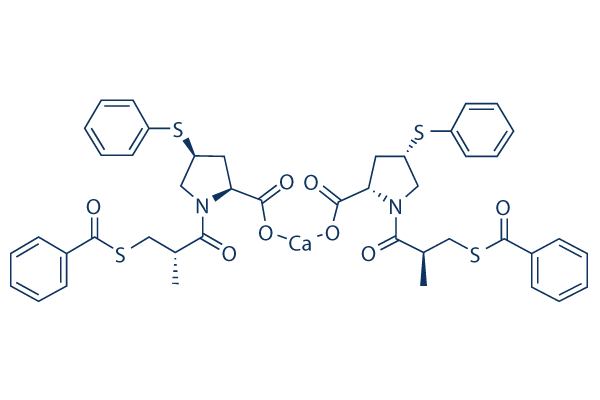
Chemische Struktur
Molekulargewicht: 897.17
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor Estrogen/progestogen Receptor GPR Androgen Receptor Glucocorticoid Receptor ACE Progesterone Receptor Opioid Receptor PGES THR |
|---|---|
| Weitere RAAS Inhibitoren | Temocapril HCl Imidapril HCl VTP-27999 TFA Temocapril Delapril Hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 897.17 | Formel | C44H44CaN2O8S4 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 81938-43-4 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | SQ-26991 | Smiles | CC(CSC(=O)C1=CC=CC=C1)C(=O)N2CC(CC2C(=O)[O-])SC3=CC=CC=C3.CC(CSC(=O)C1=CC=CC=C1)C(=O)N2CC(CC2C(=O)[O-])SC3=CC=CC=C3.[Ca+2] | ||
Löslichkeit
|
In vitro |
DMSO
: 5.33 mg/mL
(5.94 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
ACE
|
|---|---|
| In vitro |
Im Meerschweinchenileum hemmte Zofenopril die kontraktile Reaktion auf Angiotensin I und verstärkte die kontraktile Reaktion auf Bradykinin. Die EC50 von Zofenoprilat lag im nanomolaren Bereich (1-8 nM). In Homogenaten von Aorta, Gehirn, Herz, Lunge, Niere und Serum von spontan hypertensiven Ratten (SHR) hemmte Zofenoprilat die ACE mit einer sehr ähnlichen Potenz (IC50: 0,8-2,8 nM). Zofenoprilat (0,01-1 mM) schützte die Endothelfunktion. Es hob die proapoptotischen Effekte von Doxorubicin auf, förderte die Mitose von bovinen koronaren venösen Endothelzellen (CVEC), verbesserte konzentrationsabhängig das Zellüberleben und verbesserte die VEGF-induzierte Proliferation von CVECs (5 Tage in 0,1 % Serum gehalten, um eine Stressbedingung zu imitieren). Zofenoprilat (1-100 μM) förderte auch die Angiogenese in Schweinekoronararterien. Zofenoprilat scheint die Proliferation von koronaren Endothelzellen zu begünstigen, was durch die Umkehrung der Apoptose zu Angiogenese führt.
|
| In vivo |
Bei wachen Ratten, Hunden und Affen führt die orale Verabreichung von Zofenopril (0,03-0,6 mg/kg) zu einer dosisabhängigen Hemmung der Pressorreaktion auf Angiotensin I. Es antagonisiert die Wirkungen von Angiotensin II oder anderen Spasmogenen nicht. Bei 2K-1C-Ratten erzeugt Zofenopril einen dosisabhängigen antihypertensiven Effekt von langer Dauer (>17 h). Bei 6,6 mg/kg senkte Zofenopril den Blutdruck um bis zu 70 mmHg (220 auf 150 mmHg). Bei SHRs hat Zofenopril dosisabhängige Effekte, die den Blutdruck um 21-33 mmHg senken. Bei der höchsten verwendeten Dosis senkt Zofenopril den Blutdruck für mindestens 17 h. Die Effekte der wiederholten Verabreichung von 22 mg/kg Zofenopril b.i.d. wurden bei SHRs evaluiert. Der systolische Blutdruck (SBP) sank am 14. Tag der Studie um 47 mmHg (188 auf 141 mmHg). Die Dauer des Effekts war länger als 12 h, da identische SBP-Werte sowohl 1 als auch 12 h nach der Arzneimittelverabreichung aufgezeichnet wurden. Basierend auf der Urinausscheidung nach oraler und i.v. Verabreichung wurde die orale Absorption von Zofenopril bei Ratten und Hunden auf über 80 % und bei Affen auf 70 % geschätzt. Die Bioverfügbarkeit von Zofenoprilat nach einer oralen Dosis von Zofenopril betrug 100 % bei Ratten, >70 % bei Hunden und 50 % bei Affen. Basierend auf einem Vergleich der AUC-Werte nach oraler und i.v. Verabreichung betrug die orale Absorption von [14C]Zofenopril bei Hunden 100 % und die Bioverfügbarkeit von Zofenoprilat 93 %. Nach einer oralen Verabreichung von Zofenopril lagen die Tmax-Werte für Zofenoprilat zwischen 0,3-0,9 h und die T1/2-Werte zwischen 5–7 h für jede der drei Tierarten. Bei Hunden, die Zofenopril intraarteriell, intravenös, intraportal oder oral erhielten, wurden 95 % der oral verabreichten Dosis von Zofenopril während des ersten Passes hydrolysiert.
|
Literatur |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
