nur für Forschungszwecke
Gabapentin HCl GABA Receptor Agonist
Kat.-Nr.S1338
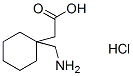
Chemische Struktur
Molekulargewicht: 207.7
Qualitätskontrolle
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- Datenblatt
- SDS
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere GABA Receptor Inhibitoren | Dihydromyricetin CGP52432 Oxiracetam Ginkgolide A Pentylenetetrazol 4-Aminobutyric acid (GABA) Emamectin Benzoate Nefiracetam Piracetam Bemegride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 207.7 | Formel | C9H17NO2.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 60142-95-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Neurontin HCl | Smiles | C1CCC(CC1)(CC(=O)O)CN.Cl | ||
Löslichkeit
|
In vitro |
Water : 42 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
GABA receptor
|
|---|---|
| In vitro |
Gabapentin unterdrückt ektope afferente Entladungsaktivität, die von verletzten peripheren Nerven erzeugt wird. Gabapentin in einem Bereich von 30 bis 90 mg/kg lindert signifikant die Allodynie bei nervenverletzten Ratten. Gabapentin hemmt dosisabhängig die ektope Entladungsaktivität von 15 verletzten Ischiasnerven-Afferenzfasern durch eine Wirkung auf die Impulsgenerierung. Gabapentin hemmt den durch KCl (30 mM) ausgelösten spannungsabhängigen Ca(2+)-Einstrom. Gabapentin hemmt stark den Spitzenstrom des gesamten Zell-Ca(2+)-Kanals (I(Ba)) dosisabhängig mit einem geschätzten IC(50)-Wert von 167 nM. Die Gabapentin-Hemmung ist spannungsabhängig und erzeugt eine hyperpolarisierende Verschiebung der Stromspannungseigenschaften um ca. 7 mV und reduziert eine nicht-inaktivierende Komponente des gesamten Zellstroms, die bei relativ depolarisierten Potentialen aktiviert wird. Gabapentin aktiviert selektiv heterodimere GABAB1a-B2-Rezeptoren, aber nicht GABAB1b-B2- oder GABAB1c-B2-Rezeptoren. Gabapentin aktiviert selektiv präsynaptische GABAB-Heterorezeptoren an glutamatergen Terminals, aber nicht GABAB-Autorezeptoren an GABAergen Terminals. Es wurde festgestellt, dass Gabapentin sowohl die exzitatorische synaptische Übertragung in vitro als auch die neuronale Reaktion auf schädliche elektrische und mechanische Stimulation in vivo, die durch α-Amino-3-hydroxy-5-methyl-4-isoxazolpropionsäure (AMPA) vermittelt wird, hemmt, aber nicht die durch N-Methyl-D-Aspartat (NMDA)-Rezeptoren vermittelten. Gabapentin wirkt als AMPA-Rezeptorantagonist im Rückenmark der Ratte, um seinen spinalen antinozizeptiven Effekt auszuüben. Gabapentin unterdrückt, während NMDA die präsynaptische Fasererregung in der CA1-Region von Hippocampus-Schnitten der Ratte verstärkte. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04613024 | Not yet recruiting | Weight Loss|Pain Postoperative |
Stanford University |
July 1 2023 | Early Phase 1 |
| NCT05276089 | Not yet recruiting | Opioid Use |
Dr Yu Fu|Teesside University|NIHR Applied Research Collaboration for North East and North Cumbria|North East Academic Health Science Network|Newcastle University |
February 1 2023 | Not Applicable |
| NCT05609682 | Recruiting | Post Operative Pain |
University of Oklahoma |
November 29 2022 | Early Phase 1 |
| NCT05750875 | Completed | Pruritus|Uremia|Chronic Kidney Diseases |
King Edward Medical University |
May 1 2022 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
