nur für Forschungszwecke
Naftopidil DiHCl Adrenergic Receptor Antagonist
Kat.-Nr.S1387
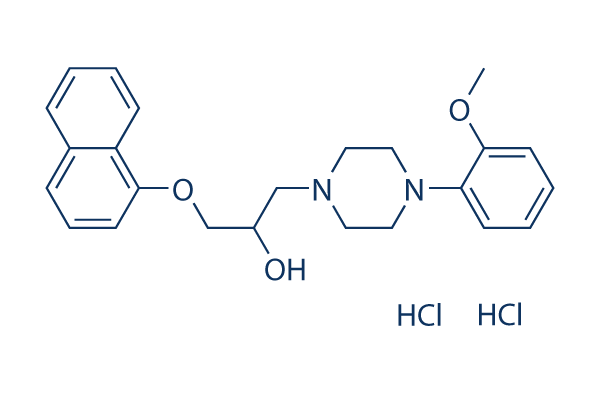
Chemische Struktur
Molekulargewicht: 465.41
Qualitätskontrolle
| Verwandte Ziele | AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Adrenergic Receptor Inhibitoren | ICI 118551 Hydrochloride (Zenidolol) L755507 Yohimbine HCl Atipamezole Naftopidil Detomidine HCl Higenamine hydrochloride Adrenalone HCl Medetomidine HCl Deoxycorticosterone acetate |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 465.41 | Formel | C24H28N2O3.2HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 57149-08-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Flivas, KT-611, Avishot,BM-15275 | Smiles | COC1=CC=CC=C1N2CCN(CC2)CC(COC3=CC=CC4=CC=CC=C43)O.Cl.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 41 mg/mL
(88.09 mM)
Ethanol : 2 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Higher selectivity for the -1A and -1D subtypes.
|
|---|---|
| Targets/IC50/Ki |
5-HT1A
0.1 μM
α1-adrenergic receptor
0.2 μM
|
| In vitro |
Naftopidil diHCl besitzt 5-HT1A-agonistische Eigenschaften und ist außerdem ein α1-adrenoceptor antagonist. Naftopidil hat eine wachstumshemmende Wirkung in Androgen-sensitiven und -insensitiven menschlichen Prostatakrebszelllinien. Naftopidil hemmt das Wachstum von Androgen-sensitiven LNCaP-Zellen und Androgen-insensitiven PC-3-Zellen mit einer IC50 von 22,2 μM bzw. 33,2 μM. Die Zellwachstumshemmung durch Naftopidil ist auf den Arrest des G1-Zellzyklus zurückzuführen. Die Expressionen von p27kip1 und p21cip1 sind in LNCaP-Zellen, die mit Naftopidil behandelt wurden, signifikant erhöht. In PC-3-Zellen induziert Naftopidil p21cip1, aber nicht p27kip1. Naftopidil bewirkt eine konzentrationsabhängige Hemmung der kollageninduzierten Ca2+-Mobilisierung, wobei die maximale Hemmung (22,9%) bei 40 μM Naftopidil auftritt. Der Adrenalin-induzierte Anstieg von [Ca2+]i wird dosisabhängig durch Naftopidil gehemmt. Naftopidil ist signifikant wirksamer als Tamsulosin bei der Linderung von Nykturie. Naftopidil induziert einen G(1)-Zellzyklusarrest sowohl in PCa-Zellen als auch in PrSC. In Naftopidil-behandelten PrSC ist das gesamte Interleukin-6-Protein signifikant reduziert, mit erhöhter Unterdrückung der Zellproliferation. |
| In vivo |
Die orale Verabreichung von Naftopidil an Nacktmäuse hemmt das Wachstum von PC-3-Tumoren im Vergleich zu Vehikel-behandelten Kontrollen. Naftopidil verbessert die Blasenkapazität und entspanntes Wasserlassen durch Hemmung der afferenten Nervenaktivität. Naftopidil (0,1 μg–30 μg) hebt isovolumetrische rhythmische Blasenkontraktionen vorübergehend auf. Die Amplitude der Blasenkontraktion wird durch intrathekale Injektion von Naftopidil (3 μg–30 μg) verringert. Naftopidil hemmt selektiv den Phenylephrin-induzierten Anstieg des Prostatadrucks im Vergleich zum mittleren Blutdruck im anästhesierten Hundemodell. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
