nur für Forschungszwecke
Ramelteon MT Receptor Agonist
Kat.-Nr.S1259
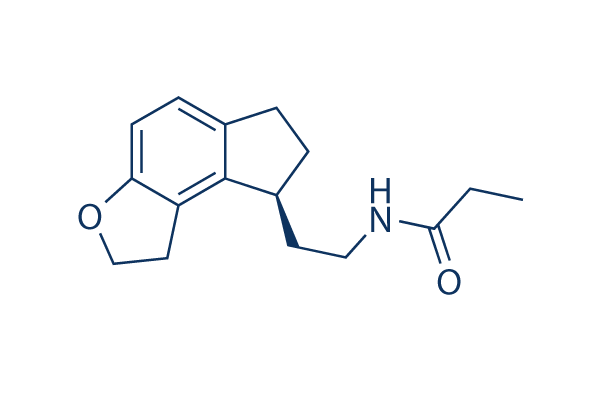
Chemische Struktur
Molekulargewicht: 259.34
Qualitätskontrolle
| Verwandte Ziele | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Weitere MT Receptor Inhibitoren | Melatonin Luzindole |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 259.34 | Formel | C16H21NO2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 196597-26-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | TAK-375 | Smiles | CCC(=O)NCCC1CCC2=C1C3=C(C=C2)OCC3 | ||
Löslichkeit
|
In vitro |
DMSO
: 51 mg/mL
(196.65 mM)
Ethanol : 51 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
A tricyclic synthetic analog of melatonin.
|
|---|---|
| Targets/IC50/Ki |
MT1 receptor
(Cell-free assay) 14 pM(Ki)
MT receptor (chicken)
(Cell-free assay) 23.1 pM(Ki)
MT2 receptor
(Cell-free assay) 112 pM(Ki)
|
| In vitro |
Ramelteon hemmt die Forskolin-stimulierte cAMP-Produktion mit einem IC50 von 21,2 pM in CHO-Zellen. Diese Verbindung hat eine hohe Affinität zu rekombinanten menschlichen MT1- und MT2-Rezeptoren mit einem pKi von 10,05 bzw. 9,70. Sie hemmt die Aggregation von Pigmentgranula in Xenopus laevis Melanophoren mit einem pEC50 von 11,48. Diese Chemikalie (1 nM) erhöht die ERK1/2-Phosphorylierung nicht nur in MT1/MT2-Kleinhirnkörnerzellen, sondern auch in Kleinhirnkörnerzellen, die nur einen der beiden Melatoninrezeptoren exprimieren. 4P-PDOT blockiert die stimulierende Wirkung dieser Verbindung (1 nM) in MT1-KO-Kleinhirnkörnerzellen, während Luzindol die Wirkung dieser Chemikalie (1 nM) in MT2-KO-Kleinhirnkörnerzellen abschwächt. Es (100 μM) induziert keine Pigmentdispersion, während Melatonin aggregierte Melanophoren bei 10 μM vollständig dispergiert.
|
| In vivo |
Ramelteon (10 mg/kg, i/p) reduziert signifikant die NREM-Schlaflatenz bei Ratten und führt auch zu einem kurzzeitigen Anstieg der Dauer des Non-REM-Schlafs (NREM), aber das NREM-Leistungsspektrum ist unverändert. Diese Verbindung (0,1 mg/kg und 1 mg/kg, p.o.) beschleunigt die Wiedereinstellung des Laufrad-Aktivitätsrhythmus an den neuen Licht-Dunkel-Zyklus bei Ratten, ohne das Lernen oder Gedächtnis zu beeinflussen. Es (0,03 mg/kg und 0,3 mg/kg, p.o.) verkürzt signifikant die Latenz bis zum Schlafbeginn und erhöht signifikant die Gesamtschlafdauer bei frei beweglichen Affen, ohne das allgemeine Verhalten der Affen zu beeinflussen.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03931070 | Completed | Delirium |
Rhode Island Hospital |
May 9 2019 | Phase 4 |
| NCT02560324 | Completed | Tobacco Use Disorder |
University of Pennsylvania|National Institute on Drug Abuse (NIDA)|National Institutes of Health (NIH) |
September 2015 | Phase 2 |
| NCT02969343 | Completed | Central Line-Associated Bloodstream Infection (CLABSI)|Venous Thromboembolism|Patient Fall|Catheter-Associated Infection|Severe Hypoglycemia|Opioid-Related Severe Adverse Drug Event|Hospital Acquired Pressure Ulcer|Adverse Drug Event|Severe Hospital Acquired Delerium|Rapid Response Related to Arrhythmia |
Brigham and Women''s Hospital|Northeastern University |
April 2015 | Not Applicable |
| NCT00568789 | Completed | Insomnia |
Takeda |
June 2006 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
