nur für Forschungszwecke
VX-809 (Lumacaftor) CFTR Modulator
Kat.-Nr.S1565

Chemische Struktur
Molekulargewicht: 452.41
Qualitätskontrolle
| Verwandte Ziele | CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase GluR |
|---|---|
| Weitere CFTR Inhibitoren | Tezacaftor (VX-661) VX-445 (Elexacaftor) Vanzacaftor (VX-121) VX-561(CTP-656) CFTRinh-172 GLPG1837 FDL169 Galicaftor (ABBV-2222) GlyH-101 IOWH032 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| CFBE41o | Corrector assay | 24 hrs | Corrector activity at CFTR F508-del mutant (unknown origin) expressed in human CFBE41o cells harboring HS-YFP preincubated for 24 hrs followed by forskolin/genistein stimulation for 30 mins by fluorescence assay, EC50 = 2.5704 μM. | 29272749 | ||
| FRT | Corrector assay | 25 mins | Corrector activity at human CFTR F508 deletion mutant expressed in FRT cells incubated for 25 mins with forskolin by YFP-based fluorescence analysis relative to control, EC50 = 2.6 μM. | 26561003 | ||
| TC32 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for TC32 cells | 29435139 | |||
| U-2 OS | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for U-2 OS cells | 29435139 | |||
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| DAOY | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for DAOY cells | 29435139 | |||
| Saos-2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| BT-37 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-37 cells | 29435139 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for RD cells | 29435139 | |||
| SK-N-SH | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| MG 63 (6-TG R) | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| NB1643 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB1643 cells | 29435139 | |||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for BT-12 cells | 29435139 | |||
| OHS-50 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| fibroblast cells | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for control Hh wild type fibroblast cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh41 cells | 29435139 | |||
| Rh30 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh30 cells | 29435139 | |||
| U-2 OS | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for U-2 OS cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh41 cells | 29435139 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for RD cells | 29435139 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| SK-N-MC | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| NB-EBc1 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB-EBc1 cells | 29435139 | |||
| LAN-5 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| Rh18 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh18 cells | 29435139 | |||
| CFBE41o | Corrector assay | 1 uM | 24 hrs | Corrector activity at CFTR F508-del mutant (unknown origin) expressed in human CFBE41o cells harboring HS-YFP assessed as increase in matured protein levels at cell surface at 1 uM after 24 hrs by electrophoretic mobility assay | 29272749 | |
| HBE | Corrector assay | Corrector activity at CFTR F508del/F508del mutant in primary HBE cells assessed as increase in chloride ion current across apical membrane measured 18 to 24 hrs post compound treatment on basolateral side of cells in presence of channel potentiator GLPG18 | 29251932 | |||
| CFBE41o | Corrector assay | Corrector activity at CFTR F508del mutant (unknown origin) expressed in human CFBE41o cells assessed as increase in fully glycosylated protein by western blot analysis | 26041577 | |||
| CFBE41o | Corrector assay | 1 uM | 24 hrs | Corrector activity at CFTR F508del mutant (unknown origin) expressed in human CFBE41o cells assessed as increase in size of cAMP-dependent current at 1 uM after 24 hrs measured at +100 mV by whole cell patch clamp assay | 26041577 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 452.41 | Formel | C24H18F2N2O5 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 936727-05-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | VRT 826809 | Smiles | CC1=C(N=C(C=C1)NC(=O)C2(CC2)C3=CC4=C(C=C3)OC(O4)(F)F)C5=CC(=CC=C5)C(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 90 mg/mL
(198.93 mM)
Ethanol : 13 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Higher specificity and efficacy relative to other CFTR defect drugs.
|
|---|---|
| Targets/IC50/Ki |
F508del-CFTR
(Fisher rat thyroid cells) 0.1 μM(EC50)
|
| In vitro |
Lumacaftor (VX-809) wirkt auf der Ebene des ER, um einem Teil des F508del-CFTR eine korrekt gefaltete Form anzunehmen, das ER zu verlassen und zur Zelloberfläche zu mobilisieren, um normal zu funktionieren. In Fischer-Ratten-Schilddrüsenzellen (FRT), die F508del-CFTR exprimieren, verbessert diese Verbindung die F508del-CFTR-Reifung signifikant um das 7,1-fache mit einer EC50 von 0,1 μM und verstärkt den F508del-CFTR-vermittelten Chloridtransport um etwa das 5-fache mit einer EC50 von 0,5 μM, während VRT-768 höhere EC50-Werte von 7,9 μM bzw. 16 μM aufweist. In HEK-293-Zellen, die F508del-CFTR exprimieren, erhöht es (3 μM) den Austritt von F508del-CFTR aus dem ER um das 6-fache und erreicht Niveaus, die 34 % des CFTR entsprechen. In primären menschlichen bronchialen Epithelzellen (HBE) mit F508del-CFTR-Mutation erhöht der Wirkstoff die CFTR-Reifung und verstärkt die Chloridsekretion mit einer EC50 von 350 nM bzw. 81 nM, was wirksamer ist als Corr-4a und VRT-325. F508del-CFTR, korrigiert durch den Wirkstoff, weist eine Einzelkanal-Öffnungswahrscheinlichkeit von 0,39 auf, ähnlich dem normalen CFTR von 0,40. Im Gegensatz zu VX-770 ist es kein CFTR-Potentiator, da eine akute Zugabe keine Auswirkung auf die F508del-CFTR-Funktion hat. Im Gegensatz zu VRT-325 und Corr-4a verbessert es die Verarbeitung der normalen oder mutierten Formen von hERG oder P-gp sowie anderer krankheitsverursachender fehlplatzierter Proteine, einschließlich α1-Antitrypsin-Z-Mutante (E342K-α1-AT) oder N370S-β-Glucosidase, nicht, was darauf hindeutet, dass es spezifisch für CFTR ist. Es hat in Kombination mit VRT-325 oder Corr-4a eine additive Wirkung auf den CFTR-vermittelten Chloridtransport in kultivierten F508del-HBE. |
| Kinase-Assay |
F508del-CFTR-Reifung
|
|
FRT-Zellen, die F508del-CFTR stabil exprimieren, werden 48 Stunden lang mit steigenden Konzentrationen von Lumacaftor (VX-809) behandelt. Nach der Inkubation werden die Zellen in eiskalter D-PBS-Lösung (ohne Kalzium und Magnesium) geerntet und bei 1.000 × g bei 4 °C pelletiert. Die Zellpellets werden in 1 % Nonidet P-40, 0,5 % Natriumdesoxycholat, 200 mM NaCl, 10 mM Tris, pH 7,8 und 1 mM EDTA plus Proteaseinhibitor-Gemisch (1:250) 30 Minuten lang auf Eis lysiert. Die Lysate werden 10 Minuten lang bei 10.000 × g bei 4 °C zentrifugiert, um Zellkerne und unlösliches Material zu pelletieren. Etwa 12 μg Gesamtprotein werden in Laemmli-Puffer mit 5 % β-Mercaptoethanol bei 37 °C 5 Minuten lang erhitzt und auf ein 3 % bis 8 % Tris-Acetat-Gel geladen. Das Gel wird auf Nitrozellulose übertragen und für das Western Blotting unter Verwendung eines monoklonalen CFTR-Antikörpers oder eines polyklonalen Antikörpers gegen GAPDH verarbeitet. Die Blots werden durch verstärkte Chemilumineszenz entwickelt. Die Quantifizierung der relativen Mengen der Banden C und GAPDH wird unter Verwendung der NIH ImageJ-Analyse gescannter Filme durchgeführt.
|
|
| In vivo |
Lumacaftor (VX-809; VRT 826809) ist ein CFTR-Modulator, der die Faltung und den Transport des CFTR-Proteins korrigiert. |
Literatur |
Anwendungen
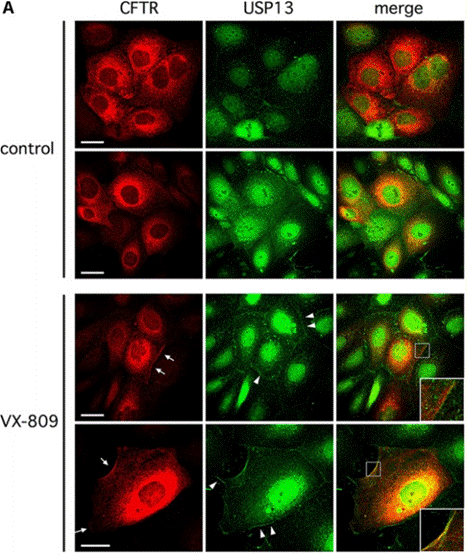
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Immunofluorescence | CFTR / USP13 Cell surface kAE1 / kAE1 |
|
30618756 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03512119 | Completed | Cystic Fibrosis Homozygous for Phe 508 Del CFTR|Glucose Intolerance or Newly Diagnosis Diabetes |
University Hospital Strasbourg France |
February 11 2016 | -- |
| NCT02589236 | Completed | Cystic Fibrosis |
Nivalis Therapeutics Inc.|Medidata Solutions |
November 2015 | Phase 2 |
| NCT02514473 | Completed | Cystic Fibrosis |
Vertex Pharmaceuticals Incorporated |
July 2015 | Phase 3 |
| NCT01899105 | Completed | Cystic Fibrosis |
Vertex Pharmaceuticals Incorporated |
July 2013 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
