nur für Forschungszwecke
Conivaptan HCl Vasopressin Receptor Antagonist
Kat.-Nr.S2116
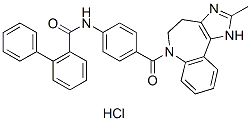
Chemische Struktur
Molekulargewicht: 535.04
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Weitere Vasopressin Receptor Inhibitoren | Mozavaptan RO 5028442 (RG7713) Lixivaptan (VPA-985) Mozavaptan (hydrochloride) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 535.04 | Formel | C32H26N4O2.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 168626-94-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | YM 087 | Smiles | CC1=NC2=C(N1)CCN(C3=CC=CC=C32)C(=O)C4=CC=C(C=C4)NC(=O)C5=CC=CC=C5C6=CC=CC=C6.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 107 mg/mL
(199.98 mM)
Ethanol : 7 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Vasopressin receptor 1
Vasopressin receptor 2
|
|---|---|
| In vivo |
Conivaptan (0,03, 0,1 und 0,3 mg/kg i.v.) erhöht dosisabhängig das Urinvolumen und reduziert die Urinosmolalität sowohl bei Myokardinfarkt- als auch bei scheinoperierten Ratten. Conivaptan (0,3 mg/kg i.v.) reduziert signifikant den rechtsventrikulären systolischen Druck, den linksventrikulären enddiastolischen Druck, das Lungen-/Körpergewicht und den rechten Vorhofdruck bei Myokardinfarkt-Ratten. Conivaptan (0,3 mg/kg i.v.) erhöht signifikant dP/dt(max)/linksventrikulären Druck bei Myokardinfarkt-Ratten. Conivaptan führt zu einer akuten Erhöhung des Urinvolumens (UV), einer Reduktion der Osmolalität (UOsm) und am Ende der Untersuchung zeigen zirrhotische Ratten, die den V(1a)/V(2)-AVP receptor antagonist erhalten, weder Hyponatriämie noch Hypoosmolalität. Conivaptan normalisiert auch U(Na)V, ohne die Kreatinin-Clearance und den arteriellen Druck zu beeinflussen. Conivaptan (0,01 bis 0,1 mg/kg i.v.) übt eine dosisabhängige diuretische Wirkung bei Hunden aus, ohne eine Zunahme der Elektrolytausscheidung im Urin, hemmt die pressorische Wirkung von exogenem Vasopressin dosisabhängig (0,003 bis 0,1 mg/kg i.v.) und blockiert bei der höchsten Dosis (0,1 mg/kg i.v.) die durch exogenes Vasopressin verursachte Vasokonstriktion nahezu vollständig. Conivaptan (0,1 mg/kg i.v.) verbessert die Herzfunktion, was durch signifikante Zunahmen von linksventrikulärem dP/dtmax, Herzzeitvolumen und Schlagvolumen belegt wird, und reduziert Vorlast und Nachlast, was durch signifikante Abnahmen des linksventrikulären enddiastolischen Drucks und des gesamten peripheren Gefäßwiderstands bei Hunden mit kongestiver Herzinsuffizienz belegt wird. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT03000283 | Completed | Cerebral Hemorrhage|Cerebral Edema|Intracerebral Hemorrhage|Stroke |
Jesse Corry|Allina Health System |
March 22 2017 | Phase 1 |
| NCT01370148 | Completed | Liver Disease |
Cumberland Pharmaceuticals |
April 2011 | Phase 1 |
| NCT00887627 | Completed | Kidney Diseases|Hyponatremia |
Cumberland Pharmaceuticals |
April 2009 | Phase 1 |
| NCT00851227 | Completed | Liver Disease|Hyponatremia |
Cumberland Pharmaceuticals |
February 2009 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
