nur für Forschungszwecke
Deoxyarbutin Tyrosinase Inhibitor
Kat.-Nr.S4132
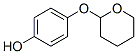
Chemische Struktur
Molekulargewicht: 194.23
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | HDAC Caspase Proteasome Secretase MMP HCV Protease Cysteine Protease DPP HIV Protease Serine Protease |
|---|---|
| Weitere Tyrosinase Inhibitoren | Aloin (Barbaloin) Arbutin Echinacoside Isorhamnetin 2-Ketoglutaric acid (alpha-ketoglutarate) Oxyresveratrol Kojic acid Hexylresorcinol 4-Chlorosalicylic acid Magnoflorine |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 194.23 | Formel | C11H14O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 53936-56-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | D-arbutin,D-Arb | Smiles | C1CCOC(C1)OC2=CC=C(C=C2)O | ||
Löslichkeit
|
In vitro |
DMSO
: 39 mg/mL
(200.79 mM)
Ethanol : 39 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
More effective than hydroquinone in inhibiting mushroom tyrosinase.
|
|---|---|
| Targets/IC50/Ki |
tyrosinase
50 nM
|
| In vitro |
DeoxyArbutin zeigt in vitro eine wirksame Hemmung der Pilz-Tyrosinase mit einem Ki, der 10-mal niedriger ist als Hydrochinon (HQ) und 350-mal niedriger als Arbutin. DeoxyArbutin zeigt Toxizität in dunkel (höhere Tyrosinase-Aktivität) und hell (geringere Tyrosinase-Aktivität) pigmentierten Melanozyten mit einer IC50 von 57,5 µM bzw. 104,7 µM. DeoxyArbutin (100 µM) hemmt die Tyrosinhydroxylase-Aktivität im Lysat von unbehandelten, dunkel pigmentierten Melanozyten dosisabhängig. DeoxyArbutin (100 µM) hemmt die Tyrosinhydroxylase-Aktivität der Pilz-Tyrosinase dosisabhängig. DeoxyArbutin hemmt die Tyrosinhydroxylase-Aktivität der Pilz-Tyrosinase mit einer IC50 von 17,5 µM und einem Ki von 21,6 µM. Wasser erhöht die Zersetzung von DeoxyArbutin in den Formulierungen, und das Polyol-in-Silikon-, Öl-basierte, wasserfreie Emulsionssystem bietet eine relativ stabile Umgebung für das DeoxyArbutin, das seinen Abbau bei 25 ℃ und 45 ℃ verzögert. DeoxyArbutin hemmt die Melanin-Synthese in intakten Melanozyten dosisabhängig. DeoxyArbutin zeigt dosisabhängige Reduzierungen der Melanozytenzellzahl, hauptsächlich aufgrund der Hemmung der Proliferation und nicht der Initiierung der Apoptose. DeoxyArbutin erhöht minimale Mengen reaktiver Sauerstoffspezies (ROS) mit anschließend induzierter Expression der endogenen Antioxidans-Katalase in behandelten Melanozyten. |
| In vivo |
DeoxyArbutin (3%) zeigt in einem haarlosen, pigmentierten Meerschweinchenmodell eine schnelle und anhaltende Hautaufhellung, die innerhalb von 8 Wochen nach Beendigung der topischen Anwendung vollständig reversibel ist. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
