nur für Forschungszwecke
Levalbuterol tartrate Adrenergic Receptor Modulator
Kat.-Nr.S3153
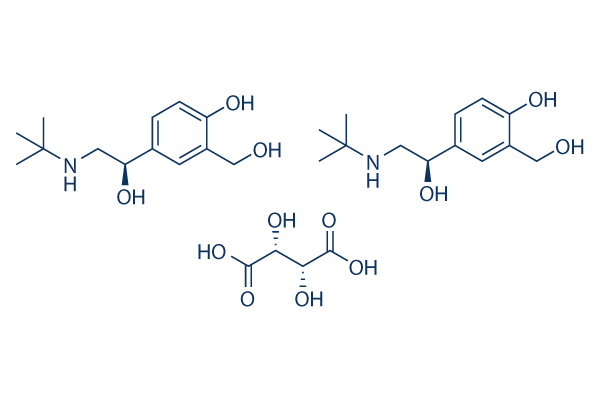
Chemische Struktur
Molekulargewicht: 628.71
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Adrenergic Receptor Inhibitoren | ICI 118551 Hydrochloride (Zenidolol) L755507 Yohimbine HCl Atipamezole Naftopidil Detomidine HCl Higenamine hydrochloride Adrenalone HCl Medetomidine HCl Deoxycorticosterone acetate |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 628.71 | Formel | C30H48N2O12 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 661464-94-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Levosalbutamol tartrate | Smiles | CC(C)(C)NCC(C1=CC(=C(C=C1)O)CO)O.C(C(C(=O)O)O)(C(=O)O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(159.05 mM)
Water : 100 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vivo |
Racemisches Albuterol (7,5 mg, zweimal täglich) führt im Vergleich zur Levalbuterol (3,75 mg, zweimal täglich)-Verabreichung bei Kindern mit Asthma nach einer Stunde kontinuierlicher Behandlung zu einer stärkeren Verbesserung des forcierten exspiratorischen Volumens in 1 Sekunde (FEV1) sowie der Asthmasymptome. Die stärkere Verbesserung der Asthmasymptome bleibt nach der zweiten Stunde der kontinuierlichen Therapie in der racemischen Albuterol-Gruppe erhalten, jedoch nicht bei den Messungen des forcierten exspiratorischen Volumens in 1 Sekunde (FEV1). Levalbuterol (1,25 mg) erfordert im Vergleich zur racemischen Albuterol (2,5 mg)-Gruppe bei Patienten mit Asthma oder chronisch obstruktiver Lungenerkrankung (COPD) signifikant weniger mediane Gesamtvernebelungen und geplante Vernebelungen. Die Bewertung der Krankheitssymptome und die allgemeinen Wohlbefinden-Scores der Probanden verbessern sich sowohl in den Levalbuterol (1,25 mg)- als auch in den racemischen Albuterol (2,5 mg)-Behandlungsgruppen signifikant gegenüber dem Ausgangswert, und die mittleren Scores für Beta-vermittelte Nebenwirkungen sind unter Levalbuterol signifikant höher als unter racemischem Albuterol. |
Literatur |
|
|---|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
