nur für Forschungszwecke
PD123319 Angiotensin Receptor Antagonist
Kat.-Nr.S7098
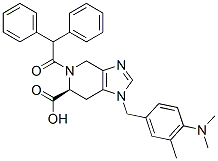
Chemische Struktur
Molekulargewicht: 508.61
Qualitätskontrolle
| Verwandte Ziele | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Weitere Angiotensin Receptor Inhibitoren | ML221 A-779 Fimasartan Olodanrigan (EMA401) Buloxibutid AVE 0991 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 508.61 | Formel | C31H32N4O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 130663-39-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C(C=CC(=C1)CN2C=NC3=C2CC(N(C3)C(=O)C(C4=CC=CC=C4)C5=CC=CC=C5)C(=O)O)N(C)C | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(196.61 mM)
Water : 100 mg/mL Ethanol : 100 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
AT2 receptor
34 nM
|
|---|---|
| In vitro |
PD 123319 diskriminiert zwischen zwei Unterklassen von AII-Rezeptoren in vielen verschiedenen Geweben. 125I-AII markierte spezifisch zwei Klassen von Bindungsstellen für AII in einer Membranpräparation von Rinder-Nebennieren-Glomerulosa-Zellen. Die erste Klasse (DuP-753-sensitiv) repräsentiert etwa 85 % der gesamten Bindungsstellen für AII und besitzt eine hohe Affinität (IC50 von 92,9 nM) für DuP-753. PD-123319 hat keinen Einfluss auf die 125I-AII-Bindung an diese Stelle. Die zweite Klasse von Bindungsstellen ist empfindlicher gegenüber PD-123319, mit einer IC50 von 6,9 nM, und hat eine viel geringere Affinität für DuP-753 (IC50 um 10 μM).
|
| In vivo |
PD 123319 hat keinen Einfluss auf die Autoregulation des zerebralen Blutflusses. Eine akute AT2-Rezeptorblockade beeinflusst die CBF-Autoregulation nicht. Die intravenöse Verabreichung von PD 123319 an wache hypertensive Ratten führt zu einem sofortigen dosisabhängigen Anstieg des MAP, der bei 3 mg/kg PD 123319 etwa 7,4 Minuten anhält.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
