nur für Forschungszwecke
Chelerythrine Chloride (NSC 646662) PKC Inhibitor
Kat.-Nr.S1292
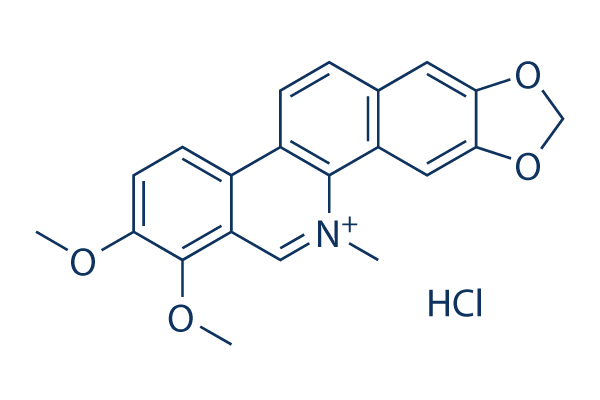
Chemische Struktur
Molekulargewicht: 384.83
Qualitätskontrolle
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 384.83 | Formel | C21H18NO4.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 3895-92-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Broussonpapyrine chloride | Smiles | C[N+]1=C2C(=C3C=CC(=C(C3=C1)OC)OC)C=CC4=CC5=C(C=C42)OCO5.[Cl-] | ||
Löslichkeit
|
In vitro |
DMSO
: 3 mg/mL
(7.79 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Chelerythrine is at least 100-fold more selective for PKCs than for other kinases.
|
|---|---|
| Targets/IC50/Ki |
PKC
(Cell-free assay) 0.66 μM
|
| In vitro |
Chelerythrine Chloride (NSC 646662) interagiert mit der katalytischen Domäne von PKC, ist ein kompetitiver Inhibitor bezüglich des Phosphatakzeptors (Histon IIIS) mit einem Ki-Wert von 0,7 μM und ein nicht-kompetitiver Inhibitor bezüglich ATP. Es zeigt potente zytotoxische Wirkungen gegen L-1210-Zellen mit einer IC50 von 0,53 μM. Diese Verbindung verändert keine Aktivität von PKA, TPK und Ca/CM-PK, und ihre hemmende Wirkung auf die PKC-Aktivität variiert nicht zwischen den verschiedenen Substraten, einschließlich GS, MLC, MBP und Fibrinogen. Es hemmt die PKC-Aktivität in Rohextrakten von SQ-20B-Zellen dosisabhängig. Chelerythrine verringert die Zellviabilität, bestimmt durch den MTT-Assay, dosisabhängig in SCC35-, JSQ3-, SQ20B- und SCC61-Zellen. Bei 5 μM unterdrückt es die VEGF-induzierte Expression von ICAM-1, VCAM-1 und E-Selektin in HUVECs. Es unterdrückt auch die VEGF-induzierte NF-κB-Aktivität in HUVECs bei gleicher Konzentration und unterdrückt sowohl die basale als auch die VEGF-induzierte Leukozytenadhäsion in HUVECs. Bei Konzentrationen von 6 mM-30 mM induziert es schnell Pyknose, Schrumpfung und den anschließenden Zelltod in Herzmuskelzellen. Chelerythrin (30 μM)-induzierter Myozyten-Tod wird von nukleärer Fragmentierung und Aktivierung von Caspase-3 und -9 in der Primärkultur neonataler Rattenherzmuskelzellen begleitet. Bei 10 μM führt es zur Freisetzung von Cytochrom c aus Mitochondrien, was darauf hindeutet, dass ROS die Chelerythrin-induzierte Cytochrom c-Freisetzung in Herzmuskelzellen vermittelt. Es verdrängt das fluoreszent markierte BH3-Domänenpeptid von einem rekombinanten GST-BcLXL-Fusionsprotein mit einer IC50 von 1,5 μM. Bei 2,5 μM und 5 μM für 16 Stunden induziert es eine erhebliche Abnahme des mitochondrialen Potentials, angezeigt durch einen Anstieg der JC-1-Grünfluoreszenz in menschlichen Neuroblastom-SH-SY5Y-Zellen. Bei 5 μM induziert es auch das Auftreten von Sub-G1-DNA, was auf Apoptose in SH-SY5Y-Zellen hinweist. Bei 10 μM induziert es eine Veränderung des mitochondrialen Potentials und die CytC-Freisetzung aus den Mitochondrien in SH-SY5Y-Zellen. |
| Kinase-Assay |
Assay für Proteinkinase C
|
|
Die gereinigte Proteinkinase C wird aus Rattenhirn präpariert. Kurz gesagt, das Inkubationsgemisch (200 μL) enthält 20 mM Tris/HCl-Puffer (pH 7,5), 10 mM MgCl2, 200 μg/mL Histone, Mizellen, hergestellt mit 700 μM Phosphatidylserin und 180 μM 1,2-Diolefin in 0,3% Triton X100, 0,2 mM CaCl2, 100 μM ATP, [γ-32P ]-ATP (105 dpm), Chelerythrine Chloride (NSC 646662) (in Dimethylsulfoxid gelöst) und das Enzym (0,5 μg Protein). Nach Inkubation bei 30℃ für 3 Minuten wird die Reaktion durch Zugabe von 3 mL 20%iger Trichloressigsäure beendet. Säurepräzipitierbare Materialien werden auf Whatman GFE-Filtern gesammelt und ausgiebig mit eiskalter 20%iger Trichloressigsäure gewaschen. Die Radioaktivität auf den Filtern wird mit einem Flüssigkeitsszintillationszähler gemessen. Die Proteinkinase C-Aktivität wird für unspezifische Aktivität korrigiert, indem der Assay in Abwesenheit von Mizellen und CaCl2 durchgeführt wird.
|
|
| In vivo |
Chelerythrine Chloride (NSC 646662) (5 mg/kg i.p.) führt zu einer Verzögerung des Tumorwachstums bei Mäusen mit SQ-20B-Xenografts. Diese Verbindung (5 mg/kg) führt zu einer signifikanten Zunahme TUNEL-positiver Kerne im Myokard sowie gespaltener Formen von Caspase-3 und -9 bei erwachsenen Ratten. |
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
