nur für Forschungszwecke
Eltrombopag Olamine TpoR Agonist
Kat.-Nr.S2229
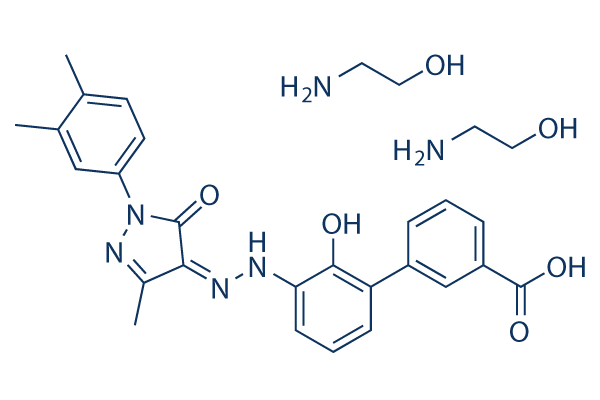
Chemische Struktur
Molekulargewicht: 564.63
Qualitätskontrolle
| Verwandte Ziele | PD-1/PD-L1 CXCR STING AhR Immunology & Inflammation related CD markers Interleukins Anti-infection Antioxidant COX |
|---|---|
| Weitere TpoR Inhibitoren | Butyzamide |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 564.63 | Formel | C29H36N6O6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 496775-62-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | SB497115,SB-497115-GR | Smiles | CC1=C(C=C(C=C1)N2C(=O)C(=C(N2)C)N=NC3=CC=CC(=C3O)C4=CC(=CC=C4)C(=O)O)C.C(CO)N.C(CO)N | ||
Löslichkeit
|
In vitro |
DMSO
: 89 mg/mL
(157.62 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
thrombopoietin receptor
|
|---|---|
| In vitro |
Eltrombopag zeigt eine halbmaximale effektive Konzentration (EC50) von 0,27 μM in murinen BAF3-Zellen, die mit dem Luciferase-Reportergen unter der Kontrolle des STAT-aktivierten IRF-1-Promotors und des humanen TpoR (BAF3/IRF-1/hTpoR) transfiziert wurden. Eltrombopag aktiviert den Rezeptor durch Assoziation mit Metallionen (d.h. Zn2+) und spezifischen Aminosäuren innerhalb der transmembranären und juxtamembranären Domänen des TpoR. Eltrombopag (30 μM) führt zur Aktivierung von STAT5 in N2C-Tpo-Zellen, wie mit einem Antiphospho-STAT5-Antikörper auf Western Blots nachgewiesen wurde. Eltrombopag stimuliert die Proliferation nach einer 2-tägigen Inkubation mit einer EC50 von 0,03 μM in einem BrdU-Assay, der in BAF3/hTpoR-Zellen durchgeführt wurde. Eltrombopag induziert auch die Differenzierung von hämatopoetischen Stammzellen in vorbestimmte Megakaryozyten-Vorläuferzellen. Eltrombopag erhöht die Differenzierung von CD34+-Knochenmarkzellen zu CD41+-Megakaryozyten dosisabhängig mit einer EC50 von 0,1 μM. Eltrombopag hemmt die Proliferation von N2C-Tpo-Zellen und HEL92.1.7-Zellen mit IC50-Werten von 20,7 μg/mL und 2,3 μg/mL. Eltrombopag (20 μg/mL) führt zu einer verringerten Zellteilungsrate, einer Blockierung in der G(1)-Phase des Zellzyklus und einer erhöhten Differenzierung in menschlichen und murinen Leukämiezellen. Eltrombopag (5 μg/mL) zeigt deutliche Anzeichen von Differenzierung, signifikante Veränderungen in der Organisation der nukleären Inhalte und eine Zunahme des Zytoplasma/Kern-Verhältnisses in HL60-Zellen. Eltrombopag (5 μg/mL) verursacht einen Anstieg von CD11b, was mit einem Prämakrophagen-Zustand in U937-Zellen übereinstimmt, und führt auch zu einem Anstieg von CD11b in URE-Zellen. Eltrombopag führt zu einer dosisabhängigen Reduktion des freien intrazellulären Eisens in leukämischen Zellen in HL60-Zellen. |
| In vivo |
Eltrombopag (10 mg/kg pro Tag) erhöht die Thrombozytenzahl bei einem Schimpansen etwa 1 Woche nach der letzten Dosis um mehr als das Doppelte und bei den beiden anderen Schimpansen um etwa das 1,5-fache. Eltrombopag (1 mg/mL) verlängert das Überleben in Mausmodellen der Leukämie. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01550185 | Terminated | Adult Acute Basophilic Leukemia|Adult Acute Eosinophilic Leukemia|Adult Acute Megakaryoblastic Leukemia (M7)|Adult Acute Minimally Differentiated Myeloid Leukemia (M0)|Adult Acute Monoblastic Leukemia (M5a)|Adult Acute Monocytic Leukemia (M5b)|Adult Acute Myeloblastic Leukemia With Maturation (M2)|Adult Acute Myeloblastic Leukemia Without Maturation (M1)|Adult Acute Myeloid Leukemia With 11q23 (MLL) Abnormalities|Adult Acute Myeloid Leukemia With Del(5q)|Adult Acute Myeloid Leukemia With Inv(16)(p13;q22)|Adult Acute Myeloid Leukemia With t(16;16)(p13;q22)|Adult Acute Myeloid Leukemia With t(8;21)(q22;q22)|Adult Acute Myelomonocytic Leukemia (M4)|Adult Erythroleukemia (M6a)|Adult Pure Erythroid Leukemia (M6b)|Recurrent Adult Acute Myeloid Leukemia |
Roswell Park Cancer Institute|GlaxoSmithKline |
May 2012 | Phase 1 |
| NCT01416311 | Completed | Purpura Thrombocytopaenic Idiopathic |
Novartis Pharmaceuticals|Novartis |
December 21 2010 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
