nur für Forschungszwecke
IC-87114 PI3K Inhibitor
Kat.-Nr.S1268
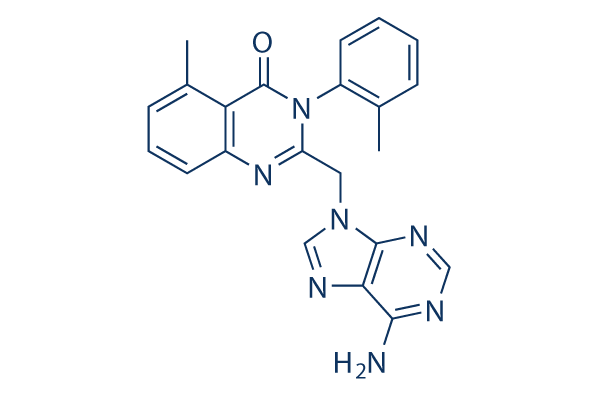
Chemische Struktur
Molekulargewicht: 397.43
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere PI3K Inhibitoren | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 397.43 | Formel | C22H19N7O |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 371242-69-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=C2C(=CC=C1)N=C(N(C2=O)C3=CC=CC=C3C)CN4C=NC5=C(N=CN=C54)N | ||
Löslichkeit
|
In vitro |
4-Methylpyridine : 10 mg/mL
DMSO
: 0.66 mg/mL
(1.66 mM)
Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PI3Kδ
(Cell-free assay) 0.5 μM
PI3Kγ
(Cell-free assay) 29 μM
|
|---|---|
| In vitro |
IC-87114 hemmt selektiv PI3Kδ und ist unempfindlich gegenüber PI3Kα, β und γ. In menschlichen Neutrophilen hemmt IC87114 (5 µM) wirksam die durch N-Formyl-Methionyl-Leucyl-Phenylalanin (fMLP) stimulierte Phosphatidylinositol-Triphosphat (PIP3)-Biosynthese und Chemotaxis. IC87114 (5 µM) hemmt auch die polarisierte Morphologie und Ausbreitung von Neutrophilen. In Blastenzellen der akuten myeloischen Leukämie (AML) beim Menschen, wie z. B. mononukleären Knochenmarkszellen (BMMCs), hemmt IC87114 (10 µM) sowohl die konstitutive als auch die durch FLT-3 stimulierte Akt-Phosphorylierung und Zellproliferation. Es wurde auch festgestellt, dass IC87114 (5 µM–30 µM) die durch SCF oder IL-3 stimulierten BMMC-Reaktionen hemmt, die in PI3Kδ-mutierten (p110δD910A) Zellen nicht beobachtet werden.
In Anti-CD3-stimulierten Mäusen hemmt IC87114 die Proliferation und Interferon-gamma (IFN-γ)-Produktion von CD62L+ (naiven) und CD62L− (Effektor-/Gedächtnis-) CD4+ T-Zellen. Die IC50-Werte von IC87114 betragen: (1) 1,2 µM und 40 nM für die CD62L+- bzw. CD62L−-Zellproliferation; (2) 120 nM und 1 nM für die IFN-γ-Produktion von CD62L+- bzw. CD62L−-Zellen. Ähnliche Wirkungen von IC87114 werden auch in menschlichen T-Zellen beobachtet. Eine aktuelle Studie zeigt, dass IC87114 in Chromaffinzellen den vorübergehenden Anstieg von PtdIns(4,5)P2 verstärkt, was zu einer Potenzierung der Exozytose führt.
|
| Kinase-Assay |
PI3K-Kinase-Assay
|
|
Es werden Phospholipid-Liposomen hergestellt, die Phosphatidylinositol-(4,5)-bisphosphat (PIP2) enthalten. Kurz gesagt werden Rinder-PIP2 und Phosphatidylserin (Molverhältnis 1:2) vakuumgetrocknet und bei 1 mM PIP2 in 20 mM HEPES-KOH, pH 7,4, 50 mM NaCl und 5 mM EDTA resuspendiert. Die Lipidsuspension wird einer kurzen Ultraschallbehandlung unterzogen, gefolgt von 5 Gefrier-Auftau-Zyklen und anschließend 20 Extrusionszyklen, um die Liposomen herzustellen. Der Assay wird in 60 μL Reaktionsvolumen in 20 mM HEPES, pH 7,4, Puffer durchgeführt, der 1 nM PI3K, 1 µM PIP2, 200 µM ATP, 1 µCi [γ-32P]ATP, 5 mM MgCl2 sowie 50 µg/mL Pferde-IgG als Trägerprotein enthält. Die Reaktion wird 10 Minuten lang bei Raumtemperatur inkubiert, in 140 von 1 M K2PO4, 30 mM EDTA, pH 8,0, gestoppt, auf einer 96-Well-Polyvinylidendifluorid-Filterplatte aufgefangen und fünfmal mit 1 M K2PO4 gewaschen. Der Filter wird vollständig trocknen gelassen und die gebundene Radioaktivität quantifiziert. IC87114-Verdünnungen werden in einer Endkonzentration von 1 % (w/w) DMSO getestet.
|
|
| In vivo |
Bei Mäusen hemmt IC87114 (15 mg/kg–60 mg/kg) die allergische Reaktion auf der Rückenhaut und im Ohr.
Bei Mäusen, denen Anti-CD3 oder ConA verabreicht wurde, reduziert IC87114 (30 mg/kg) Überempfindlichkeitsreaktionen und senkt die Plasmaspiegel von Zytokinen wie IL-2, IL-4, IL-17, IFN-γ und Tumornekrosefaktor-α (TNF-α).
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
