nur für Forschungszwecke
Lansoprazole Proton Pump Inhibitor
Kat.-Nr.S1354
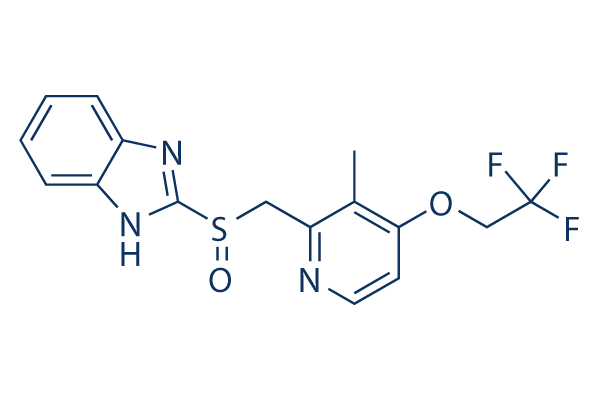
Chemische Struktur
Molekulargewicht: 369.36
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Weitere Proton Pump Inhibitoren | Bafilomycin A1 (Baf-A1) Ilaprazole Tenatoprazole Revaprazan Hydrochloride Ilaprazole sodium PF-3716556 Ufiprazole |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 369.36 | Formel | C16H14F3N3O2S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 103577-45-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | A-65006, AG-1749 | Smiles | CC1=C(C=CN=C1CS(=O)C2=NC3=CC=CC=C3N2)OCC(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 74 mg/mL
(200.34 mM)
Ethanol : 14 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Proton pump
H(+),K(+)-ATPase
|
|---|---|
| In vitro |
Lansoprazole hemmt die Magensäuresekretion durch Hemmung der gastrischen Wasserstoff/Kalium-Adenosintriphosphatase (H+,K(+)-ATPase), einem Enzym der gastrischen Parietalzellmembran, das Teil der Proton Pump ist, die den letzten Schritt im Säuresekretionsprozess durchführt. Diese Verbindung bindet kovalent an die parietale Zelle H+,K(+)-ATPase, wodurch sie funktionsunfähig wird und die Sekretion von Magensäure gehemmt wird. Es ist ein starkes antisekretorisches Mittel, das auf die gastrische H+/K+-Adenosintriphosphatase (H+/K+ ATPase) der Parietalzellen wirkt. Diese Chemikalie hemmt die erhöhte Expression von vaskulären Adhäsionsmolekülen, die Aktivierung von Neutrophilen und die Produktion von proinflammatorischen Zytokinen aus aktivierten Endothelzellen. Es induziert mehrere Gene, einschließlich des Phase-II-Entgiftungsenzyms (NADPH-Ubichinon-Oxidoreduktase, Glutathion-S-Transferase) und antioxidativer Stressproteine (HO-1, Thioredoxinreduktase und Superoxiddismutase) in Magenepithelzellen. Diese Verbindung hemmt signifikant die Produktion von CINC-1 aus stimulierten RGM-1-Zellen mit IL-1β. Es reguliert die HO-1-Expression über Nrf2 in Rattenmagenepithelzellen hoch, und die hochregulierte HO-1 hat entzündungshemmende Wirkungen.
|
| In vivo |
Lansoprazole hemmt akute Entzündungsreaktionen sowie Darmschleimhautverletzungen, die durch Ischämie-Reperfusion oder Indomethacin-Verabreichung bei Ratten induziert werden. Diese Verbindung hemmt signifikant Darmverletzungen, die durch Ischämie-Reperfusion oder Indomethacin induziert werden. Diese exogen verabreichte Verbindung schützt den Dünndarm vor Ischämie-Reperfusion oder Indomethacin-induzierten Schäden, wobei die Wirkung von ihren entzündungshemmenden und antioxidativen Reaktionen abhängt.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT02442752 | Withdrawn | Pediatric Gastroesophageal Reflux Disease |
Takeda |
June 15 2025 | Phase 1 |
| NCT03316976 | Completed | Healthy Volunteers |
Takeda |
November 22 2017 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
