nur für Forschungszwecke
CH5132799 PI3K Inhibitor
Kat.-Nr.S2699
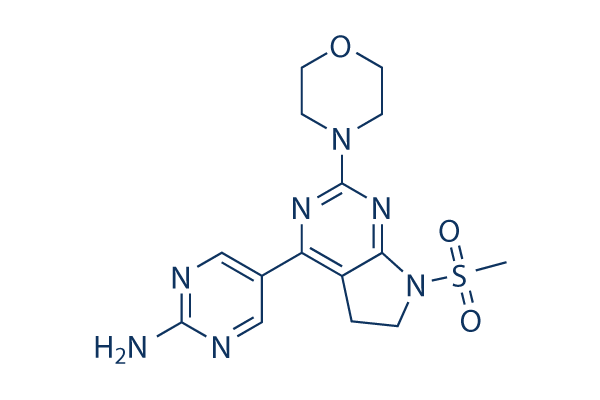
Chemische Struktur
Molekulargewicht: 377.42
Qualitätskontrolle
| Verwandte Ziele | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere PI3K Inhibitoren | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 377.42 | Formel | C15H19N7O3S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1007207-67-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | MEN1611, PA799 | Smiles | CS(=O)(=O)N1CCC2=C(N=C(N=C21)N3CCOCC3)C4=CN=C(N=C4)N | ||
Löslichkeit
|
In vitro |
DMSO
: 12 mg/mL
(31.79 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PI3Kα
14 nM
PI3Kγ
36 nM
PI3Kβ
0.12 μM
PI3Kδ
0.50 μM
|
|---|---|
| In vitro |
CH5132799 hemmt selektiv PI3K der Klasse I, PI3Kα (IC50 = 0,014 μM), PI3Kβ (IC50 = 0,12 μM), PI3Kδ (IC50 = 0,50 μM), PI3Kγ (IC50 = 0,036 μM), zeigt aber weniger Hemmung von PI3K der Klasse II, PI3k der Klasse III und mTOR und auch keine hemmende Aktivität (IC50 > 10 μM) gegen 26 Proteinkinasen. Diese Verbindung zeigt höhere hemmende Aktivitäten gegen PI3Kα mit onkogenen Mutationen E542K (IC50 = 6,7 nM), E545K (IC50 = 6,7 nM) und H1047R (IC50 = 5,6 nM) als Wildtyp-PI3Kα. Bei mit dieser Chemikalie behandelten Brustkrebs-KPL-4-Zellen, die die PIK3CA-Mutation aufweisen, werden die Phosphorylierung von Akt und seiner direkten Substrate PRAS40 und FoxO1/3a sowie die Phosphorylierung nachgeschalteter Faktoren, einschließlich S6K, S6 und 4E-BP1, effektiv unterdrückt. Krebszelllinien mit PIK3CA-Mutationen sind signifikant empfindlich gegenüber dieser Verbindung In menschlichen Tumorzelllinien mit PI3K-Signalweg-Aktivierung durch Mutation zeigt es eine potente antiproliferative Aktivität [HCT116(CRC): IC50 = 0,20 lM, KPL-4(BC):13 IC50 = 0,032 lM, T-47D(BC): IC50 = 0,056 lM, SK-OV-3(Ovarian): IC50 = 0,12 lM]. Es unterdrückt effektiv die Phosphorylierung von AKT in KPL-4-Zellen.
|
| Kinase-Assay |
PI3K Assay
|
|
Die E542K-, E545K- und H1047R-Mutanten von PI3Kα werden mittels überlappender Extensions-Polymerase-Kettenreaktion hergestellt. Glutathion-S-Transferase-markierte PI3Kα-Mutanten und His-markiertes p85α werden mit dem BAC-TO-BAC Baculovirus Expressionssystem koexprimiert. Die hemmenden Aktivitäten dieser Verbindung auf PI3Kα (p110α/p85α), PI3Kβ (p110β/p85α), PI3Kδ (p110δ/p85α), PI3Kγ (p110γ), PI3KC2α, PI3KC2β, Vps34 und PI3Kα-Mutanten werden mit dem Adapta Universal Kinase Assay Kit bestimmt. Die zeitaufgelöste Fluoreszenz wird mit einem EnVision HTS Mikrotiterplattenlesegerät gemessen. Die IC50-Werte werden mit XLfit berechnet.
|
|
| In vivo |
CH5132799 zeigt eine potente In-vivo-Antitumoraktivität in verschiedenen Xenograft-Modellen mit PIK3CA-Mutationen. Diese Verbindung überwindet die mTORC1-Hemmung-vermittelte Akt-Aktivierung und das Wiederwachstum von Xenograft-Tumoren durch Langzeitbehandlung mit Everolimus. Es ist ein klinischer Kandidat, der eine ausgezeichnete orale Bioverfügbarkeit (BA) (101% bei Mäusen), humane mikrosomale Leberstabilität und In-vivo-Antitumoraktivität im PC-3-Xenograft-Modell zeigt (TGI: 101% bei 25 mg/kg, p.o., q.d. × 11 Tage). Diese Chemikalie zeigt eine gute orale BA bei Mäusen, Ratten, Affen und Hunden (F: 54,2-101%). In einem humanen Brustkrebs (KPL-4: PI3Ka H1047R) Xenograft-Modell bei Mäusen zeigt die orale Behandlung mit dieser Verbindung (12,5 mg/kg, q.d.) eine starke Tumorregression. Die starke Regression bleibt während der 6-wöchigen Verabreichung erhalten, selbst bei intermittierender Dosierung (q.d., 2 Wochen an/1 Woche aus; q.d., 5 Tage an/2 Tage aus), was darauf hindeutet, dass ein flexibler Verabreichungsplan in der Klinik anwendbar sein könnte.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01222546 | Completed | Solid Tumors |
Chugai Pharma Europe Ltd. |
August 2010 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
