nur für Forschungszwecke
Muramyl dipeptide (MDP) RUNX Aktivator
Kat.-Nr.S9709
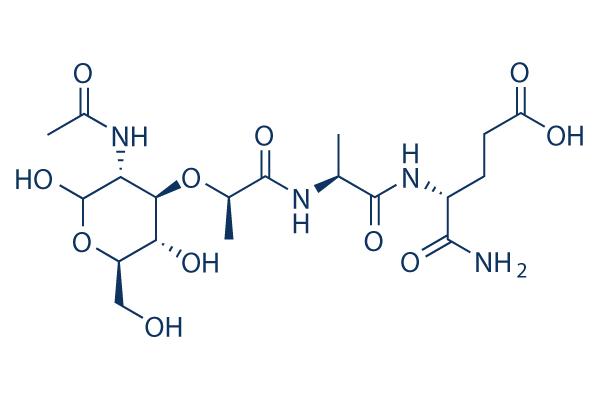
Chemische Struktur
Molekulargewicht: 492.48
Qualitätskontrolle
| Verwandte Ziele | CDK HSP PD-1/PD-L1 ROCK Wee1 DNA/RNA Synthesis Microtubule Associated Ras KRas Aurora Kinase |
|---|---|
| Weitere RUNX Inhibitoren | CADD522 XRK3F2 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 492.48 | Formel | C19H32N4O11 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 53678-77-6 | -- | Lagerung von Stammlösungen |
|
|
Löslichkeit
|
In vitro |
DMSO
: 98 mg/mL
(198.99 mM)
Water : 98 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Runx2
|
|---|---|
| In vitro |
Muramyl dipeptide (MDP) verstärkt direkt die Osteoblastendifferenzierung und die Expression von knochenbildenden Genen durch RUNX2-Aktivierung. Obwohl es keine direkte Wirkung hat, dämpft es indirekt die Osteoklastendifferenzierung durch Herunterregulierung des RANKL/OPG-Verhältnisses. Diese Verbindung erhöht die Expression ihres Rezeptors Nod2, und die MDP-induzierte Knochenbildung und Osteoblastenaktivierung treten bei Nod2-Mangel nicht auf. |
| In vivo |
Bei Mäusen, denen Muramyl dipeptide (MDP) verabreicht wurde, wird eine erhöhte Knochen- und Mineraliendichte durch verbesserte Knochenbildung beobachtet. Bemerkenswerterweise lindert die Vor- oder Nachbehandlung mit dieser Verbindung den Knochenverlust in RANKL-induzierten Osteoporose-Mausmodellen. |
Literatur |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06079567 | Recruiting | Facioscapulohumeral Muscular Dystrophy Type 2 |
Centre Hospitalier Universitaire de Nice |
October 3 2023 | Not Applicable |
| NCT06045338 | Not yet recruiting | Long COVID|Post-Acute Sequelae of COVID-19|COVID Long-Haul |
Beth Israel Deaconess Medical Center |
October 2023 | Not Applicable |
| NCT06110403 | Recruiting | Copd |
University Hospital Lille|AstraZeneca |
September 29 2023 | Phase 1|Phase 2 |
| NCT06012006 | Not yet recruiting | COPD |
Assistance Publique - Hôpitaux de Paris |
August 2023 | Not Applicable |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
