nur für Forschungszwecke
JPH203 (Nanvuranlat) LAT1-Inhibitor
Kat.-Nr.S8667
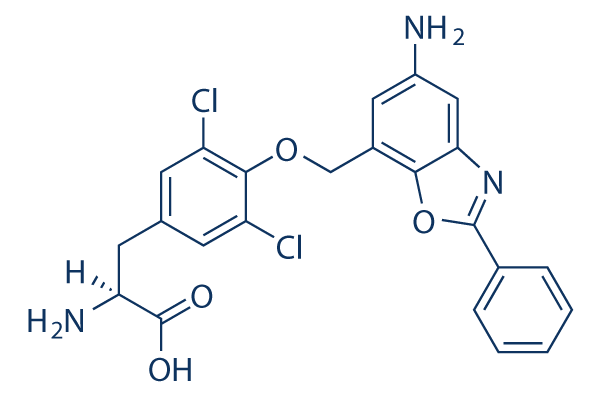
Chemische Struktur
Molekulargewicht: 472.32
Qualitätskontrolle
| Verwandte Ziele | CFTR CRM1 CD markers AChR Calcium Channel Sodium Channel Potassium Channel GABA Receptor TRP Channel ATPase |
|---|---|
| Weitere Amino acid transporter Inhibitoren | V-9302 GPNA hydrochloride BCH |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HT-29 | Function assay | 1 hr | Inhibition of [14C]-L-leucine uptake at LAT1 in human HT-29 cells after 1 hr by liquid scintillation counting, IC50=0.06μM. | 27253989 | ||
| YD-38 | Function assay | 1 hr | Inhibition of [14C]-L-leucine uptake at LAT1 in human YD-38 cells after 1 hr by liquid scintillation counting, IC50=0.79μM. | 27253989 | ||
| HT-29 | Growth inhibition assay | 96 hrs | Growth inhibition of human HT-29 cells measured after 96 hrs by Coulter counter based cell counting method, IC50=4.1μM. | 27253989 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 472.32 | Formel | C23H19Cl2N3O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1037592-40-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | KYT-0353, JPH-203SBECD | Smiles | C1=CC=C(C=C1)C2=NC3=CC(=CC(=C3O2)COC4=C(C=C(C=C4Cl)CC(C(=O)O)N)Cl)N | ||
Löslichkeit
|
In vitro |
5%TFA : 2.31 mg/mL
DMSO
: 0.01 mg/mL
(0.02 mM)
Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
LAT1
(Cell-free assay) |
|---|---|
| In vitro |
Nanvuranlat (JPH203) hemmte die L-Leucin-Aufnahme in YD-38-Zellen (IC50-Wert: 0,79 μM) bzw. NHOKs (IC50-Wert: >100 μM) vollständig und leicht. Es hemmte das Wachstum von HT-29-Zellen und erzeugte einen scheinbaren IC50 von 4,1 μM, aber die zur Hemmung der L-Leucin-Aufnahme benötigte IC50-Konzentration (0,06 μM) hemmte das Wachstum von HT-29-Zellen nicht, was einen 68-fachen Unterschied in der Empfindlichkeit darstellt. Diese Verbindung aktivierte den Mitochondrien-abhängigen apoptotischen Signalweg durch Hochregulierung pro-apoptotischer Faktoren wie Bad, Bax und Bak und der aktiven Form von Caspase-9 sowie durch Herunterregulierung anti-apoptotischer Faktoren wie Bcl-2 und Bcl-xL in menschlichen Saos2-Osteosarkomzellen. Es kann die relative Häufigkeit zwischen LAT1 und LAT2 unterscheiden und weist eine hohe Selektivität für LAT1 auf. JPH203 war in Lebermikrosomeninkubationen von Maus, Ratte, Hund, Affe und Mensch metabolisch stabil. Es induziert sowohl einen G2/M- als auch einen G0/G1-Zellzyklusarrest und reduzierte die S-Phase, begleitet von einer veränderten Expression der Proteine im Zellzyklusverlauf: Cyclin D1, CDK4 und CDK6.
|
| In vivo |
Die tägliche intravenöse Verabreichung von JPH203 (12,5 und 25 mg/kg) hemmte das Tumorwachstum in KKU-213-Cholangiokarzinomzell-Xenografts im Nacktmausmodell dosisabhängig signifikant, ohne statistisch signifikante Änderungen des Körpergewichts der Tiere und ohne Unterschiede in der Histologie und dem Aussehen der inneren Organe im Vergleich zur Kontrollgruppe. Somit zeigt diese Verbindung eine Antitumorwirksamkeit in Nacktmäusen, die menschliche Cholangiokarzinom (CCA)-Zell-Xenografts tragen, ohne allgemeine Toxizität.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p53 / Bad / Bcl-2 / Bcl-xl / Bax / Bak / Cleaved caspase / Cleaved PARP p70S6K / p-P70S6k / p-S6 / S6 / p-ERK / ERK / p-AKT / AKT' p-GCN2 / GCN2 / p-EIF2α / EIF2α / ATF4 |
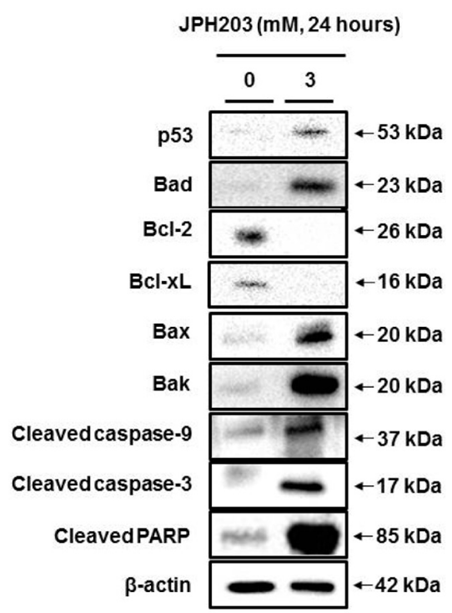
|
29200902 |
| Growth inhibition assay | Cell viability |
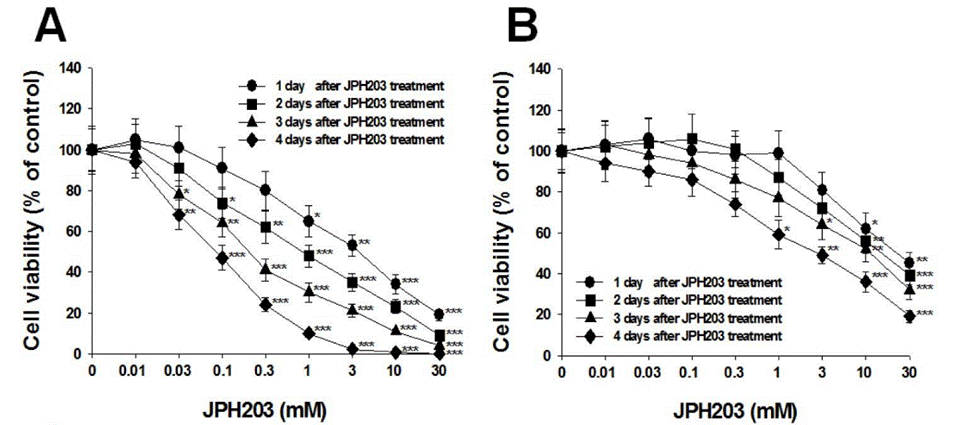
|
29200902 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
