nur für Forschungszwecke
Ozanimod S1P Receptor Modulator
Kat.-Nr.S7952
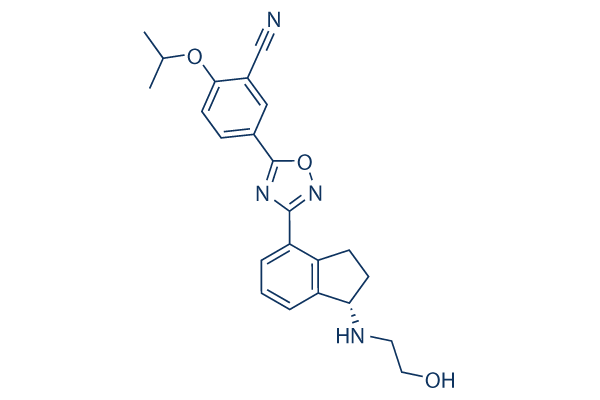
Chemische Struktur
Molekulargewicht: 404.46
Qualitätskontrolle
| Verwandte Ziele | CXCR Hedgehog/Smoothened PKA Adrenergic Receptor AChR 5-HT Receptor Histamine Receptor Dopamine Receptor Ras KRas |
|---|---|
| Weitere S1P Receptor Inhibitoren | JTE 013 PF 429242 CAY10444 CYM5541 CYM-5520 SEW 2871 SLF1081851 hydrochloride CYM50308 MP-A08 Etrasimod(APD334) |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 404.46 | Formel | C23H24N4O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1306760-87-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | RPC1063 | Smiles | CC(C)OC1=C(C=C(C=C1)C2=NC(=NO2)C3=C4CCC(C4=CC=C3)NCCO)C#N | ||
Löslichkeit
|
In vitro |
DMSO
: 40 mg/mL
(98.89 mM)
Ethanol : 10 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
S1P1R
(Cell-free assay) 0.41 nM(EC50)
S1P5R
(Cell-free assay) 11 nM(EC50)
|
|---|---|
| In vitro |
In S1P1R-HEK293T-Zellen induziert Ozanimod eine anhaltende S1P1R-Internalisierung und -Degradation. |
| Kinase-Assay |
In-vitro-Pharmakologie-Assays
|
|
Zellsignalisierungs-Assays verwendeten den LiveBLAzer-FRET B/G-Assay, um cAMP (S1P1R) oder β-Arrestin-Signalisierung (S1P4R) nachzuweisen. Die Assays werden in 384-Well-Platten in dreifacher Ausführung gemäß den Herstelleranweisungen durchgeführt. Verbindungslösungen werden bei 10 mM in 100 % DMSO bei -80 °C gelagert und anfänglich 1:10 mit 20 % (2-Hydroxypropyl)-β-Cyclodextrin verdünnt. Eine 10-Punkt-Dosis-Wirkungs-Kurve wird bei 40-facher Endassaykonzentration in 10 mM Hepes pH 7,4, enthaltend 0,1 % Pluronic F-127, erstellt. Für den S1P1R-Assay werden 80 μM Forskolin in das Verdünnungsmittel gegeben. Kurz gesagt, 104 Zellen/Well werden 4 Stunden lang bei 37 °C mit einer Dosis-Wirkungs-Reihe des Liganden inkubiert. CC4-AM-Substrat und Probenecid werden zugegeben und 2 weitere Stunden bei 37 °C inkubiert und mit einem SpectramaxM5 analysiert. Für S1P1R-cAMP-Assays werden die Daten auf die maximale Fluoreszenz, die durch 2 μM Forskolin erzeugt wird, normalisiert. Für GTPγS-Bindungsassays werden 1-5 μg/Well Membranprotein mit 10 μM GDP, 100-500 μg/Well Wheat Germ Agglutinin PVT SPA-Beads in 50 mM HEPES, 100 mM NaCl, 10 mM MgCl2, 20 μg/ml Saponin und 0,1 % fettsäurefreiem BSA für 15 Minuten in 96-Well-Platten inkubiert. Nach Zugabe der Verbindung und 200 pM GTP [35S] (1250 Ci/mmol) werden die Platten 120 Minuten lang inkubiert und bei 300 g für 5 Minuten zentrifugiert. Die Radioaktivität wird mit einem TopCount-Instrument nachgewiesen. Alle Daten werden mit einer nichtlinearen Regression mit variabler Steigung (GraphPad Prism) an ein Vier-Parameter-Modell angepasst, um die halbmaximale effektive Konzentration (EC50) und die maximale Wirksamkeit relativ zu S1P zu erzeugen.
|
|
| In vivo |
In vivo zeigt Ozanimod eine hohe orale Bioverfügbarkeit und ein hohes Verteilungsvolumen. In einem MOG-induzierten EAE-Mausmodell unterdrückt diese Verbindung (3 mg/kg, p.o.) klinische Symptome. In einem Ratten-TNBS-Modell für entzündliche Darmerkrankungen hemmt sie (1,2 mg/kg, p.o.) klinische und histologische Krankheitswerte. In einem naiven CD4+CD45Rbhi T-Zell-Adoptivtransfermodell reduzierte diese Chemikalie (1,2 mg/kg, p.o.) auch die Krankheitschwere signifikant, beurteilt durch Messung des Entzündungsgrades, des Drüsenverlusts, der Hyperplasie, des Neutrophileninfiltrats und der Schleimhautdicke. |
Literatur |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06408259 | Not yet recruiting | Multiple Sclerosis Relapsing-Remitting |
Celgene |
July 9 2024 | Phase 3 |
| NCT06334094 | Not yet recruiting | Multiple Sclerosis |
The University of Texas at Dallas|Texas Institute for Neurological Disorders |
June 1 2024 | Phase 4 |
| NCT06188637 | Not yet recruiting | Ulcerative Colitis |
Geert D''Haens|Bristol-Myers Squibb|Academisch Medisch Centrum - Universiteit van Amsterdam (AMC-UvA) |
March 1 2024 | Phase 4 |
| NCT05470985 | Recruiting | Crohn Disease |
Bristol-Myers Squibb |
August 22 2023 | Phase 2|Phase 3 |
| NCT05811416 | Recruiting | Relapsing-remitting Multiple Sclerosis (RRMS) |
Bristol-Myers Squibb |
June 14 2023 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
