nur für Forschungszwecke
Gedatolisib (PKI-587) PI3K Inhibitor
Kat.-Nr.S2628
Chemische Struktur
Molekulargewicht: 615.73
Qualitätskontrolle
| Verwandte Ziele | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere PI3K Inhibitoren | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| MDA-MB-361 cells | Cytotoxicity assay | Cytotoxicity against human MDA-MB-361 cells, IC50=0.004 μM | ||||
| PC3MM2 cells | Cytotoxicity assay | Cytotoxicity against human PC3MM2 cells, IC50=0.0131 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt T308 phosphorylation in human MDA-MB-361 cells by Western blotting, IC50=0.008 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt S473 phosphorylation in human MDA-MB-361 cells by Western blotting, IC50=0.01 μM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of eNOS phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of PARS40 phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of GSK3 kinase phosphorylation in human MDA-MB-361 cells by Western blotting | ||||
| MDA-MB-361 cells | Function assay | Inhibition of mTOR TORC1 kinase activity in human MDA-MB-361 cells assessed as suppression of p70S6K phosphorylation at < 30 nM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of mTOR TORC1 kinase activity in human MDA-MB-361 cells assessed as suppression of 4EBP1 phosphorylation at < 30 nM | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt T308 phosphorylation in human MDA-MB-361 cells xenografted mouse model upto 36 hrs | ||||
| MDA-MB-361 cells | Function assay | Inhibition of Akt S473 phosphorylation in human MDA-MB-361 cells xenografted mouse model upto 36 hrs | ||||
| MDA-MB-361 cells | Function assay | Induction of PARP cleavage in human MDA-MB-361 cells xenografted mouse model upto 18 hrs | ||||
| MDA-MB-361 cells | Function assay | Antitumor activity against human MDA-MB-361 cells xenografted mouse model assessed as reduction in tumor volume at 20 mg/kg, iv on day 1, 5, 9 | ||||
| SF9 insect cells | Function assay | 2 h | Inhibition of human PI3Kalpha expressed in SF9 insect cells after 2 hrs by fluorescence polarization assay, IC50=0.0004 μM | |||
| SF9 insect cells | Function assay | 2 h | Inhibition of human PI3Kgamma expressed in SF9 insect cells after 2 hrs by fluorescence polarization assay, IC50=0.011μM | |||
| MDA-MB-361 cells | Growth inhibition assay | 72 h | Growth inhibition of human MDA-MB-361 cells after 72 hrs, IC50=0.003 μM | |||
| human PC3 cells | Growth inhibition assay | 72 h | Growth inhibition of human PC3 cells after 72 hrs, IC50=0.011 μM | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 615.73 | Formel | C32H41N9O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1197160-78-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | PF-05212384 | Smiles | CN(C)C1CCN(CC1)C(=O)C2=CC=C(C=C2)NC(=O)NC3=CC=C(C=C3)C4=NC(=NC(=N4)N5CCOCC5)N6CCOCC6 | ||
Löslichkeit
|
In vitro |
DMSO
: 3 mg/mL
(4.87 mM)
Ethanol : 1 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PI3Kα
(Cell-free assay) 0.4 nM
mTOR
(Cell-free assay) 1.6 nM
PI3Kγ
(Cell-free assay) 5.4 nM
|
|---|---|
| In vitro |
Gedatolisib (PKI-587) zeigt eine starke hemmende Aktivität gegen PI3K-α, PI3K-γ und mTOR mit IC50-Werten von 0,4 nM, 5,4 nM bzw. 1,6 nM. Darüber hinaus zeigt es auch seine Wirksamkeit gegen die am häufigsten auftretenden mutierten Formen von PI3Kα, insbesondere H1047R und E545K mit IC50-Werten von 0,6 nM bzw. 0,6 nM. In Korrelation mit der Unterdrückung der Phosphorylierung von PI3K/mTOR-Signalwegproteinen bewirkt diese Verbindung eine Hemmung des Tumorzellwachstums in den Zelllinien MDA-361 und PC3-MM2 mit IC50-Werten von 4 nM bzw. 13,1 nM.
|
| Kinase-Assay |
PI3K- und mTOR-Kinase-Assay
|
|
Enzymassays werden im Fluoreszenzpolarisation (FP)-Format durchgeführt, das an das Protokoll des Echelon K-1100 PI3K FP Assay Kits angepasst ist. Humane Klasse-I-PI3Ks und PI3K-α-Mutanten (E545K und H1047R) werden in Sf9 produziert oder von Upstate Biotech erworben. GST-GRP1 (murin) wird in Escherichia coli produziert und durch GST-Sepharose isoliert. Die Assay-Puffer sind Reaktionspuffer [20 mM HEPES (pH 7,1), 2 mM MgCl2, 0,05 % CHAPS und 0,01 % β-Mercaptoethanol] und Stopp-/Detektionspuffer [100 mM HEPES (pH 7,5), 4 mM EDTA, 0,05 % CHAPS]. Die FP-Reaktion wird 30 Minuten lang bei Raumtemperatur in 20 μL Reaktionspuffer durchgeführt, der 20 μM Phosphatidylinositol-4,5-bisphosphat (PIP2), 25 μM ATP und <4 % DMSO enthält. Die FP-Reaktion wird mit 20 μL Stopp-/Detektionspuffer (10 nM Sonde und 40 nM GST-GRP) gestoppt, und nach 2 Stunden werden die Daten mit einem Envision-Plattenlesegerät erfasst. Die Routineassays mit gereinigtem FLAG-TOR (FL und 3,5) werden in 96-Well-Platten wie folgt durchgeführt. Enzyme werden zuerst in Kinase-Assay-Puffer (10 mM Hepes (pH 7,4), 50 mM NaCl, 50 mM β-Glycerophosphat, 10 mM MnCl2, 0,5 mM DTT, 0,25 μM Microcystin LR und 100 μg/mL BSA) verdünnt. Zu jeder Vertiefung werden 12 μL des verdünnten Enzyms kurz mit 0,5 μL Testinhibitor oder Kontrollvehikel Dimethylsulfoxid (DMSO) gemischt, wobei der Testinhibitor Gedatolisib (PKI-587) ist. Die Kinase-Reaktion wird durch Zugabe von 12,5 μL Kinase-Assay-Puffer, der ATP und His6-S6K enthält, eingeleitet, um ein Endreaktionsvolumen von 25 μL zu erhalten, das 800 ng/mL FLAG-TOR, 100 μM ATP und 1,25 μM His6-S6K enthält. Die Reaktionsplatte wird 2 Stunden (linear bei 1–6 Stunden) bei Raumtemperatur unter sanftem Schütteln inkubiert und dann durch Zugabe von 25 μL Stopp-Puffer (20 mM Hepes (pH 7,4), 20 mM EDTA und 20 mM EGTA) beendet.
|
|
| In vivo |
Die Behandlung mit Gedatolisib (PKI-587) bei 25 mg/kg i.v. bei Nacktmäusen führt zu einer geringen Plasmaclearance (7 (mL/min)/kg), einem hohen Verteilungsvolumen (7,2 L/kg) und einer langen Halbwertszeit (14,4 Stunden). Im MDA-361-Xenograft-Modell zeigt es eine starke Antitumorwirksamkeit mit der minimal wirksamen Dosis (MED) von 3 mg/kg gegen MDA-361-Tumoren und der maximal verträglichen Einzeldosis (MTD) von 30 mg/kg. Im H1975 (nicht-kleinzelliges Lungenkarzinom, mutiertes EGFR [L858R, T790M])-Xenograft-Modell führt diese Verbindung bei 25 mg/kg über 7 Wochen zu einer Überlebensrate von 90 % in der behandelten Gruppe.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Growth inhibition assay | Cell viability |
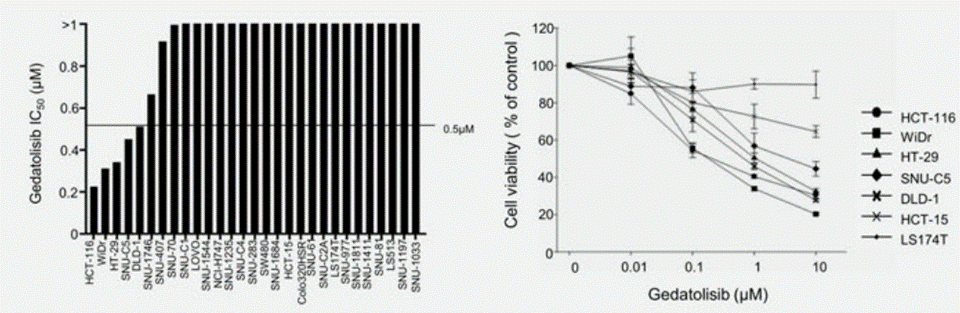
|
29978469 |
| Western blot | p-AKT / p-mTOR / p-p70S6K / p-S6K / p-4E-BP1 / AKT / mTOR / p70S6K / S6K / 4EBP1 TSC1 / TSC2 / Raptor |
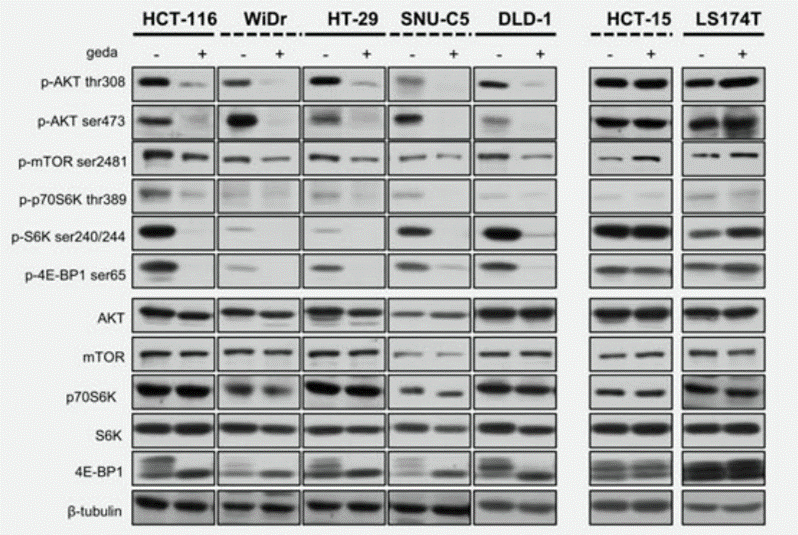
|
29978469 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT02438761 | Terminated | Therapy-related Acute Myeloid Leukemia and Myelodysplastic Syndrome|Acute Myeloid Leukemia in Relapse|de Novo Acute Myeloid Leukemia at Diagnostic |
Institut Curie|Fondation ARC|National Cancer Institute France |
August 31 2015 | Phase 2 |
| NCT02069158 | Completed | Breast Cancer|NSCLC|Ovary Cancer|Endometrial Cancer|Small Cell Lung Cancer (SCLC)|Head and Neck (HNSCC) |
Cristiana Sessa|Oncology Institute of Southern Switzerland |
April 2014 | Phase 1 |
| NCT01420081 | Terminated | Endometrial Neoplasms |
Pfizer |
January 19 2012 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
