nur für Forschungszwecke
PYR-41 E1 Activating Inhibitor
Kat.-Nr.S7129
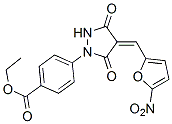
Chemische Struktur
Molekulargewicht: 371.3
Qualitätskontrolle
| Verwandte Ziele | Proteasome E3 Ligase DUB p97 SUMO E2 conjugating |
|---|---|
| Weitere E1 Activating Inhibitoren | MLN4924 (Pevonedistat) TAK-243 (MLN7243) ML792 TAS4464 DKM 2-93 COH000 NEDD8 inhibitor M22 Pevonedistat hydrochloride PYZD-4409 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HI5 insect cells | Function assay | 30 min | Inhibition of N-terminal GST-tagged human UAE-catalyzed UAE-Ub thioester intermediate formation expressed in HI5 insect cells after 30 mins by immunoblotting analysis, IC50=10 μM | |||
| HI5 insect cells | Function assay | Inhibition of N-terminal GST-tagged human UAE-catalyzed [32P]-AMP:[a-32P]-ATP exchange expressed in HI5 insect cells by TLC analysis, IC50=6.4 μM | ||||
| insect cells | Function assay | Inhibition of mouse recombinant His6-tagged UAE-catalyzed UAE-Ub thioester intermediate formation expressed in insect cells by SDS-PAGE analysis, IC50=10 μM | ||||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 371.3 | Formel | C17H13N3O7 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 418805-02-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCOC(=O)C1=CC=C(C=C1)N2C(=O)C(=CC3=CC=C(O3)[N+](=O)[O-])C(=O)N2 | ||
Löslichkeit
|
In vitro |
DMSO
: 74 mg/mL
(199.29 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Ubiquitin-activating Enzyme E1
(Cell-free assay) <10 μM
|
|---|---|
| In vitro |
PYR-41 (50 μM) hemmt die Aktivität des Ubiquitin-aktivierenden Enzyms E1 um über 90%. Diese Verbindung könnte ein Ziel für nukleophilen Angriff sein und potenziell mit dem aktiven Zentrum-Cystein von E1 reagieren. Es blockiert effizient den Cyclin E-Abbau. Diese Chemikalie senkt den Spiegel von E1fUb-Thioestern in Zellen mit einer IC50 zwischen 10 und 25 μM und verhindert die durch Proteasom-Inhibitoren induzierte Akkumulation ubiquitylierter Proteine. Es erhöht die Gesamt-Sumoylierung in Zellen und in Zellen, die temperaturempfindliches E1 enthalten. Es ist in der Lage, sowohl Proteasom-abhängige als auch Proteasom-unabhängige Aktivitäten der Ubiquitylierung zu hemmen. Diese Verbindung (50 μM) schwächt die 1 ng/mL IL-1α-vermittelte Aktivierung des nukleären Faktors-κB um >60% ab, indem sie die nachgeschaltete Ubiquitylierung und den proteasomalen Abbau von IκBα verhindert. Es hemmt den Abbau von p53 und aktiviert die transkriptionelle Aktivität von p53, was es ermöglicht, transformierte p53-exprimierende Zellen differenziell abzutöten.
Es blockiert Ubiquitinierungsreaktionen, führt aber paradoxerweise zur Akkumulation von hochmolekularen ubiquitinierten Proteinen. Diese Verbindung hat auch eine gleiche oder größere hemmende Aktivität gegen mehrere Deubiquitinasen (DUBs) in intakten Zellen und gereinigtem USP5 in vitro. Es vermittelt auch die Quervernetzung spezifischer Proteinkinasen (Bcr-Abl, Jak2), um deren Signalaktivität zu hemmen.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
