nur für Forschungszwecke
Wortmannin (SL-2052) PI3K Inhibitor
Kat.-Nr.S2758
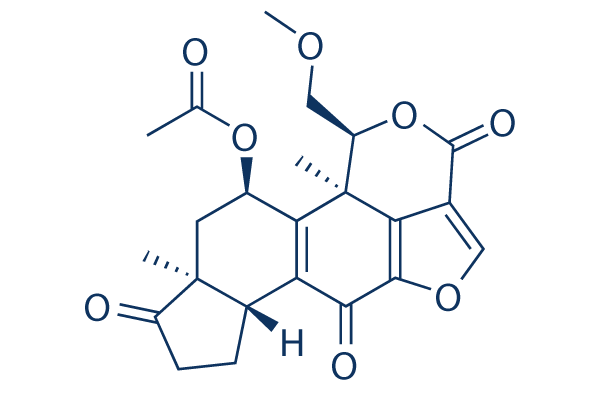
Chemische Struktur
Molekulargewicht: 428.43
Qualitätskontrolle
| Verwandte Ziele | Akt mTOR GSK-3 ATM/ATR DNA-PK AMPK PDPK1 PTEN PP2A PDK |
|---|---|
| Weitere PI3K Inhibitoren | GDC-0077 (Inavolisib) SAR405 Quercetin (Sophoretin) LY294002 XL147 analogue Tersolisib (STX-478) Buparlisib (BKM120) 740 Y-P (PDGFR 740Y-P) GO-203 TFA Eganelisib (IPI-549) |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| Mel-HO | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| A-375-TS | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| A-375 | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| Huh7 | Function Assay | 3 μM | 1 h | reduces the virus entry into the cells | 24184196 | |
| BEL/FU | Function Assay | 1 mM | 24 h | decreases protein levels of the PI3K/Akt pathway | 24232099 | |
| HCT 116 | Function Assay | 100 nM | 24 h | attenuates the colonies of the tumor cells with upregulation of Akt1 | 24297510 | |
| HepG2 | Function Assay | 100 nM | 24 h | attenuates the colonies of the tumor cells with upregulation of Akt1 | 24297510 | |
| SW480 | Function Assay | 150nM | 20 h | DMSO | reduces cellular accumulation of β-catenin | 24324366 |
| HEK-293 | Function Assay | 150nM | 16 h | DMSO | decreases CRT activity | 24324366 |
| 5637 | Apoptosis Assay | 10 μM | 40 min | reverses p21WAF1 expression, CDK expression, and cell inhibition induced by fucoidan | 24333868 | |
| MG-63 | Apoptosis Assay | 10 µM | 12 h | enhances DP-induced apoptosis | 24358301 | |
| H1975 | Function Assay | 10 μM | 1 h | DMSO | decreases cellular phospho-AKT protein levels | 24447935 |
| H520 | Function Assay | 10 μM | 1 h | DMSO | decreases cellular phospho-AKT protein levels | 24447935 |
| HepG2 | Function Assay | 200 nM | 0.5 h | attenuates FoxO phosphorylation | 24535192 | |
| HL-60 | Function Assay | 0.1 μM | 72 h | blocks cell differentiation | 24607273 | |
| SK-N-LO | Function Assay | 100 nM | 0.5 h | decreases the stimulant effects of on Akt phosphorylation | 24654606 | |
| A549 | Function Assay | 10 μm | 16 h | DMSO | modulates the IAV replication and causes retention of NP in the nucleus. | 24802111 |
| A549 | Growth Inhibition Assay | 3 µM | 2 h | suppresses Akt and GSK3β activation, S-phase arrest, cell apoptosis and caspase-3 activation | 24847863 | |
| HepG2 | Function Assay | 100 nM | 0.5 h | DMSO | blocks MA-induced Akt phosphorylation | 24863350 |
| MO59J | Apoptosis Assay | 10 μM | 24 h | DMSO | increases the DSB level induced by or | 24953561 |
| MO59K | Apoptosis Assay | 10 μM | 24 h | DMSO | increases the DSB level induced by or | 24953561 |
| MO59J | Cytotoxicity Assay | 5 μM | 7 d | DMSO | enhances the cytotoxicity of or | 24953561 |
| MO59K | Cytotoxicity Assay | 5 μM | 7 d | DMSO | enhances the cytotoxicity of or | 24953561 |
| HT-29 | Growth Inhibition Assay | 1.5 µM | 96 h | decreases cell growth which can be inhibited by KYNA | 25012123 | |
| MCF7 | Function Assay | 100 nM | 24 h | eliminates E2-induced ARE-Luc activity | 25172557 | |
| MDA-MB-231 | Apoptosis Assay | 1 μM | 48 h | DMSO | decreases the cell survival treated with 25 μM of F1 or F2 | 25300932 |
| APRE-19 | Apoptosis Assay | 5 μM | 24 h | abolishes FLZ-mediated pro-survival/anti-apoptosis activity | 25329617 | |
| HUVECs | Cytotoxicity Assay | 100 nM | 24 h | attenuates the abrogative effects of calycosin on VRI-induced cytotoxicity | 25450186 | |
| H1703 | Growth Inhibition Assay | 2.5 μM | 1-4 d | DMSO | enhances cell growth inhibition treatment with | 25490383 |
| A459 | Growth Inhibition Assay | 2.5 μM | 1-4 d | DMSO | enhances cell growth inhibition treatment with | 25490383 |
| Mel-HO-TS | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| MeWo | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| Mel-2a | Apoptosis Assay | 4/8 μM | 24 h | enhances TRAIL-induced apoptosis | 24113173 | |
| MDA-MB-231 | Function Assay | 0–400 nM | 4 h | suppresses Akt phosphorylation in a dose-dependent manner | 22906259 | |
| MDA-MB-231 | Function Assay | 400 nM | 4 h | decreases MMP-9 and IL-8 protein in a dose-dependent manner | 22906259 | |
| Jurkat | Growth Inhibition Assay | 0.25-1.25 μM | 24/48 h | DMSO | inhibits cell proliferation in both time- and dose- dependent manner | 19757185 |
| Namalwa | Growth Inhibition Assay | 0.25-1.25 μM | 24/48 h | DMSO | inhibits cell proliferation in both time- and dose- dependent manner | 19757185 |
| Jurkat | Apoptosis Assay | 0.25-1.25 μM | 24/48 h | DMSO | induces cell apoptosis in both time- and dose- dependent manner | 19757185 |
| Namalwa | Apoptosis Assay | 0.25-1.25 μM | 24/48 h | DMSO | induces cell apoptosis in both time- and dose- dependent manner | 19757185 |
| K562 | Growth Inhibition Assay | 24 h | IC50=25±0.14 nM | 19662361 | ||
| SW1990 | Function Assay | 0.01-1 μM | 1 h | inhibits HA-induced Akt phosphorylation | 19469020 | |
| RT112 | Growth Inhibition Assay | 10 μM | 24 h | DMSO | decreases the proportion of G2/M cells | 18787832 |
| MHG-U1 | Growth Inhibition Assay | 10 μM | 24 h | DMSO | decreases the proportion of G2/M cells | 18787832 |
| SMMC-7721 | Apoptosis Assay | 200 nM | 24 h | increases CHX-induced apoptosis | 17557191 | |
| SMMC-7721 | Function Assay | 200 nM | 24 h | up-regulates β1,4GT1 expression | 17557191 | |
| HeLa | Function Assay | 100 nM | 1 h | alters the morphology of the transferrin recycling compartment | 16890915 | |
| MRC5VI | Function Assay | 12.5 mM | 0.5 h | DMSO | abolishes the Ser473/Thr308 phosphorylation of AktPKB | 16227394 |
| AT5BIVA | Function Assay | 12.5 mM | 0.5 h | DMSO | abolishes the Ser473/Thr308 phosphorylation of AktPKB | 16227394 |
| M059J | Function Assay | 12.5 mM | 0.5 h | DMSO | abolishes the Ser473/Thr308 phosphorylation of AktPKB | 16227394 |
| HeLa | Function Assay | 12.5 mM | 0.5 h | DMSO | abolishes the Ser473/Thr308 phosphorylation of AktPKB | 16227394 |
| N2a | Apoptosis Assay | 0.1-10 μM | 2 h | induces decreased cell viability in a concentration-dependent manner | 15842767 | |
| Jurkat | Kinase Assay | IC50 of 24 nM | 15664519 | |||
| Sf9 | Function assay | Inhibition of human PI3Kalpha expressed in Sf9 cells by fluorescent polarization assay, IC50 = 0.012 μM. | 21121631 | |||
| HeLa | Function assay | Inhibition of AX-7503 binding to recombinant Plk3 expressed in HeLa cells by Western blot, IC50 = 0.049 μM. | 17135248 | |||
| HeLa | Function assay | Binding affinity for DNA dependent protein kinase isolated from HeLa cells; Range is 20-120, Ki = 0.12 μM. | 15658870 | |||
| HeLa | Function assay | Binding affinity for Phosphatidylinositol 3-kinase isolated from HeLa cells; Range is 20-120, Ki = 0.12 μM. | 15658870 | |||
| A549 | Function assay | Inhibition of Plk3 in human A549 cells assessed as casein substrate phosphorylation by Western blot, IC50 = 0.22 μM. | 17135248 | |||
| A549 | Antiproliferative assay | 48 hrs | Antiproliferative activity against human A549 cells after 48 hrs by SRB method, IC50 = 11.4 μM. | 18630894 | ||
| GM00637 | Function assay | 1 uM | Inhibition of recombinant Plk3 expressed in human GM00637 cells at 1 uM assessed as decrease in p53 serine-20 phosphorylation | 17135248 | ||
| MDA-MB-231 | Function assay | 1 to 10 uM | 24 hrs | Inhibition of PI3K in human MDA-MB-231 cells assessed as inhibition of AKT phosphorylation at 1 to 10 uM after 24 hrs by Western blot analysis | 24828286 | |
| HeLa | Function assay | 100 nM | 10 mins | Inhibition of PI3K in human HeLa cells assessed as reduction in EGF-stimulated AKT phosphorylation at S473 at 100 nM preincubated for 10 mins followed by EGF stimulation measured after 5 mins by Western blot analysis | 30380865 | |
| HeLa | Function assay | 100 nM | 10 mins | Inhibition of PI3K in human HeLa cells assessed as reduction in EGF-stimulated AKT phosphorylation at T308 at 100 nM preincubated for 10 mins followed by EGF stimulation measured after 5 mins by Western blot analysis | 30380865 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 428.43 | Formel | C23H24O8 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 19545-26-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | KY 12420, SL-2052, BRN 0067676, NSC 627609 | Smiles | CC(=O)OC1CC2(C(CCC2=O)C3=C1C4(C(OC(=O)C5=COC(=C54)C3=O)COC)C)C | ||
Löslichkeit
|
In vitro |
DMSO
: 85 mg/mL
(198.39 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PI3K
(Cell-free assay) 3 nM
DNA-PK
(Cell-free assay) 16 nM
ATM
(Cell-free assay) 150 nM
MLCK
(Cell-free assay) 170 nM
|
|---|---|
| In vitro |
Die Hemmung von MLCK durch Wortmannin wird nicht durch Calmodulin oder Peptidsubstrat beeinflusst, während sie durch eine hohe ATP-Konzentration reduziert wird. Diese Verbindung interagiert direkt mit der katalytischen Domäne von MLCK und führt zu einem irreversiblen Verlust der Enzymaktivität. Sie hat keine hemmende Wirkung auf cAMP-abhängige Proteinkinase, cGMP-abhängige Proteinkinase und Calmodulin-abhängige Proteinkinase II und hat nur geringe Auswirkungen auf die Proteinkinase C-Aktivität. Dieser Inhibitor hemmt die N-Formylmethionyl-Leucylphenylalanin (fMLP)-stimulierte PtdInsP3 (Phosphatidylinositol-3,4,5-Trisphosphat)-Bildung mit einer IC50 von 5 nM, und diese Hemmung wird vollständig aufgehoben, wenn menschliche Neutrophile mit 100 nM dieser Verbindung vorbehandelt werden, wobei die PtdInsP2-Spiegel erhöht sind und keine Auswirkungen auf die zellulären PtdInsP- und PtdIns-Gehalte bestehen. Es könnte oszillatorische Veränderungen im F-Aktin-Gehalt entwickeln und hemmt die fMLP-stimulierte Aktinpolymerisation in Neutrophilen nicht. Diese Chemikalie hemmt irreversibel die Phosphatidylinositol-3-Kinase (PI3-Kinase)-Aktivität durch Bindung an das 110-kDa-Protein (IC50 von 3 nM) und hat keine Wirkung auf PI4-Kinase in RBL-2H3-Zellen. Sie hemmt auch die Leukotrienfreisetzung, ohne die Aktivierung der Tyrosinkinase Lyn zu beeinflussen. Diese Verbindung unterdrückt die induzierte Hexoseaufnahme in isolierten Rattenadipozyten bei 0,1 μM vollständig, ohne die stimulierte lipolytische Aktivität zu beeinträchtigen. Es unterdrückt die induzierte Stickoxidproduktion um 50 % bei 500 nM in menschlichen Endothelzellen der Nabelvene, was eine Reaktion auf IGF-1 ist. Diese Chemikalie unterdrückt die Reparatur von DNA-Doppelstrangbrüchen (DSB) und hat keinen Einfluss auf die DSB-Spiegel oder die Kinetik der Einzelstrangbruch (SSB)-Reparatur in Chinesischen Hamster-Ovarialzellen bei 50 μM. Es könnte die durch ionisierende Strahlung (IR) induzierte Zytotoxizität verstärken, ohne selbst toxisch zu sein. Dieser Inhibitor hemmt die Polo-ähnliche Kinase (PLK1)-Aktivität mit einer IC50 von 24 nM in intakten G2/M-arretierten Zellen. Es erhöht die Toll-like Rezeptor (TLR)-vermittelte Akkumulation von IL-6 in menschlichen Makrophagen mit einer EC50 von 50 nM. Gleichzeitig verstärkt diese Verbindung die TLR-vermittelte induzierbare Stickoxid-Synthase (iNOS)-Expression und Nitritakkumulation in Mäusemakrophagen signifikant. Es aktiviert den nukleären Faktor-κB und reguliert die Zytokin-mRNA-Produktion hoch. Diese Chemikalie hemmt auch Polo-like kinase (PlK) 1 und PlK3, die wichtige Rollen bei der Mitose spielen. Ihre Behandlung könnte zu einer Reduktion der Phosphorylierung von p53 an Serin 20 führen, die durch DNA-Schäden induziert wird. Es unterdrückt die Hyaluronan-induzierte Akt-Phosphorylierung und Zellmotilität/Migration in SW1990-Zellen. |
| Kinase-Assay |
MLCK assay
|
|
Die MLCK-Aktivität wird mit Peptidsubstrat (KKRPQRATSNVFS-NH2) oder Myosin-Leichtkette bestimmt. Das Peptidsubstrat (24 μM) wird in einem Reaktionsgemisch phosphoryliert, das 25 mM Tris-HCl (pH 7,5), 0,5 mg/mL Rinderserumalbumin, 4 mM MgCl2, 0,5 mM CaCl2, 2,6 nM Calmodulin, 1,5 nM MLCK und 400 μM ATP in einem Endvolumen von 0,25 mL enthält. Nach einer 10-minütigen Vorinkubation bei 28 ºC ohne ATP wird die Reaktion durch Zugabe von ATP bei 28 ºC gestartet und nach 30 min durch Zugabe von 0,1 mL 10 % (v/v) Essigsäure beendet. Das Gemisch wird mittels Hochleistungsflüssigkeitschromatographie analysiert: Säule, Unisil Pack 5C18 4,6 x 150 mm; Lösungsmittel, 18 % (v/v) Acetonitril, 0,1 % (v/v) Trifluoressigsäure in Wasser; Flussrate, 1,0 mL/min; Temperatur, 40 ºC; Detektion, Absorption bei 220 nm. Der Reaktionsprozentsatz wird aus dem Verhältnis der Peakflächen der phosphorylierten Form zu denen der unphosphorylierten Form berechnet. Die unter den oben beschriebenen Bedingungen gemessene spezifische Aktivität beträgt 0,81 μmol/min/mg. Myosin-Leichtkette (108 μg/mL) wird in einem Reaktionsgemisch phosphoryliert, das 25 mM Tris-HCl (pH 7,5), 0,5 mg/mL Rinderserumalbumin, 4 mM MgCl2, 0,5 mM CaCl2, 4,2 nM Calmodulin, 0,92 nM Enzym und 10 μM [γ-32P]ATP (100-900 cpm/pmol) in einem Endvolumen von 0,25 mL enthält. Nach einer 3-minütigen Vorinkubation bei 30 ºC ohne ATP wird die Reaktion durch Zugabe von [γ-32P]ATP bei 30 ºC gestartet und nach 5 min durch Zugabe von 0,125 mL Trichloressigsäure gestoppt. Die säurefällbaren Materialien werden auf einem Nitrozellulosemembranfilter gesammelt und mit vier 1-mL-Aliquoten von 5 % (v/v) Trichloressigsäure gewaschen. Die Radioaktivität auf dem Filter wird in einem Toluol-Szintillationsfluid mit einem Packard Tri-Carb Flüssigszintillationsspektrometer Modell 4530 gemessen. Die unter diesen Bedingungen gemessene spezifische Aktivität beträgt 1,23 μmol/min/mg.
|
|
| In vivo |
Wortmannin hemmt die peritoneale Metastasierung von SW1990 bei Mäusen bei 1 mg/kg, ohne Gewichtsverlust. Diese Verbindung hemmt die Phosphatidylinositid-3-Kinase-Proteinkinase B (PKB)/Akt-Phosphorylierung sowohl in normalen Geweben (Lunge, Herz und Hirnhomogenate) als auch in Tumorgewebe bei Mäusen, ohne Mortalität oder akute Toxizität bei 0,7 mg/kg. In Kombination mit LY188011 erhöht diese Chemikalie signifikant die Apoptose und hemmt das Tumorwachstum bei orthotopischen Tumoren, während beide Monotherapien dies nicht konnten. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | p-AKT / AKT / p-GSK3β / GSK3β / Bcl-xl / Bax / Caspase-3 / Cleaved caspase-3 |
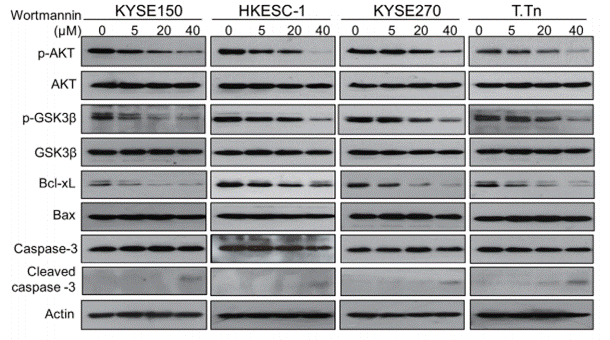
|
25344912 |
| Immunofluorescence | DNMT1 |
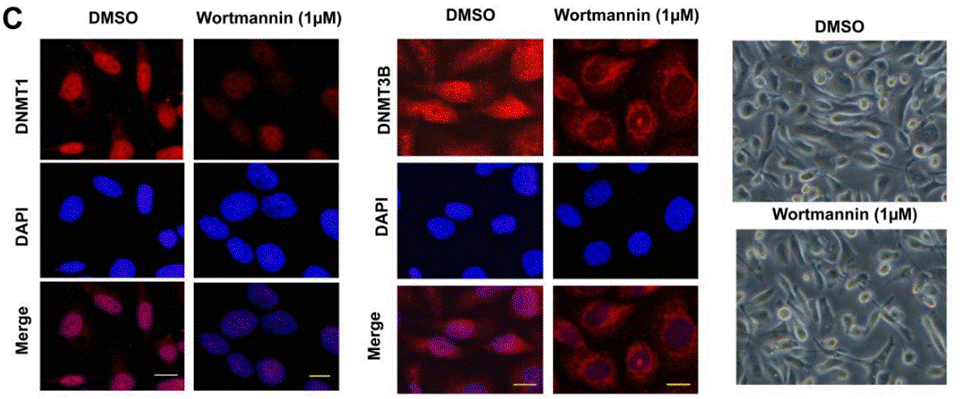
|
24001151 |
| Growth inhibition assay | Cell viability |
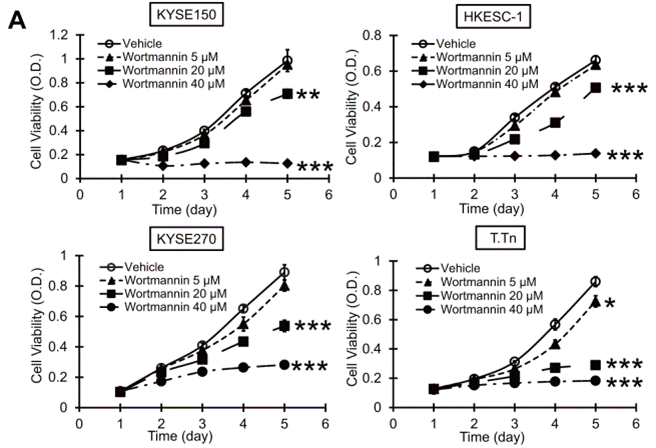
|
25344912 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
