nur für Forschungszwecke
Apixaban Factor Xa Inhibitor
Kat.-Nr.S1593
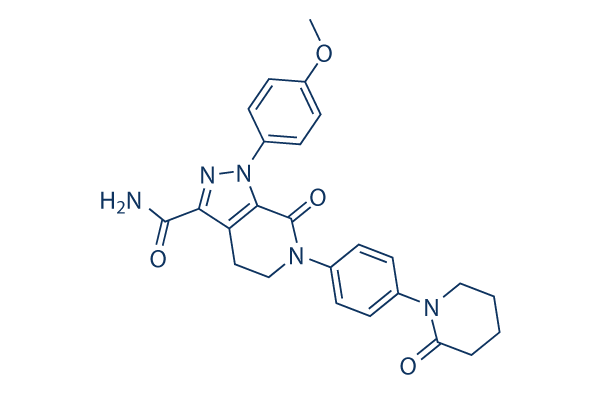
Chemische Struktur
Molekulargewicht: 459.5
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere Factor Xa Inhibitoren | Asundexian |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| A673 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| BT-37 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-37 cells | 29435139 | |||
| SJ-GBM2 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for SJ-GBM2 cells | 29435139 | |||
| Rh41 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh41 cells | 29435139 | |||
| RD | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for RD cells | 29435139 | |||
| Rh30 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Confirmatory screen for Rh30 cells | 29435139 | |||
| Caco-2 | Function assay | 48 hrs | Determination of IC50 values for inhibition of SARS-CoV-2 induced cytotoxicity of Caco-2 cells after 48 hours by high content imaging, IC50=5.91μM | ChEMBL | ||
| Caco-2 | Toxicity assay | 48 hrs | Toxicity against Caco-2 cells determined at 48 hours by intracellular ATP concentration using the CellTiter-Glo Luminescent Cell Viability Assay, CC50=18.07μM | ChEMBL | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 459.5 | Formel | C25H25N5O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 503612-47-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | BMS 562247-01 | Smiles | COC1=CC=C(C=C1)N2C3=C(CCN(C3=O)C4=CC=C(C=C4)N5CCCCC5=O)C(=N2)C(=O)N | ||
Löslichkeit
|
In vitro |
DMSO
: 18 mg/mL
(39.17 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
A highly selective, reversible, and direct factor Xa inhibitor.
|
|---|---|
| Targets/IC50/Ki |
Factor Xa (human)
(Cell-free assay) 0.08 nM(Ki)
Factor Xa (rabbit)
(Cell-free assay) 0.17 nM(Ki)
|
| In vitro |
Apixaban zeigt eine hohe Potenz, Selektivität und Wirksamkeit auf Factor Xa mit Ki von 0,08 nM und 0,17 nM für humanen Factor Xa bzw. Kaninchen Factor Xa. In vitro verlängert diese Verbindung die Gerinnungszeiten von normalem menschlichem Plasma mit Konzentrationen (EC2x) von 3,6 μM, 0,37 μM, 7,4 μM und 0,4 μM, die jeweils erforderlich sind, um die Prothrombinzeit (PT), modifizierte Prothrombinzeit (mPT), aktivierte partielle Thromboplastinzeit (APTT) und HepTest zu verdoppeln. Darüber hinaus zeigt es die höchste Potenz in menschlichem und Kaninchenplasma, aber eine geringere Potenz in Ratten- und Hundplasma sowohl in den PT- als auch in den APTT-Assays. |
| Kinase-Assay |
Enzym-Affinitäts-Assays.
|
|
Alle Enzym-Ki-Werte werden aus gereinigten menschlichen Enzymen gewonnen. Alle fXa-Assays werden in Mikrotiterplatten mit einem Gesamtvolumen von 250 μL in 0,1 M Natriumphosphatpuffer, enthaltend 0,2 M NaCl und 0,5 % Polyethylenglykol 6000 bei pH 7,0, durchgeführt. Apixaban wird bei 10 μM, 3,16 μM, 1,0 μM, 0,316 μM, 0,1 μM, 0,0316 μM, 0,01 μM und 0,00316 μM getestet. Die Platten werden 30 Minuten lang bei 405 nm abgelesen. Die Raten werden in Anwesenheit der Kontrollen (ohne Inhibitor) und für die Inhibitoren bestimmt. Diese Verbindung wird in Doppelstudien getestet und mit den gleichen internen Standards verglichen. Die Intraassay- und Interassay-Variabilität betragen 5 % bzw. 20 %. Alle Enzymassays werden in pH 7,4 Puffer bei Raumtemperatur durchgeführt. Alle Enzyme werden aus menschlichen Geweben gereinigt und stammen aus kommerziell erhältlichen Quellen. Individuelle Enzym- und Substrat-Km werden in separaten Experimenten bestimmt und liegen nahe an den in der Literatur etablierten Werten. Die Steady-State-Hemmung der Enzymaktivität wird durch Inkubation einer Reihe von Inhibitor-Konzentrationen (1 nM bis 50 μM, in Duplikaten) mit fester Enzymkonzentration (0,1 nM–100 nM) und Peptidsubstratkonzentration (200 μM–1000 μM) für bis zu 30 Minuten bestimmt. Der Ki wird unter Annahme einer kompetitiven Hemmung und einer Ein-Stellen-Bindung entweder aus dem IC50 oder aus dem Ausmaß der Hemmung bei jeder Inhibitor-Konzentration berechnet.
|
|
| In vivo |
Beim Hund zeigt Apixaban eine hervorragende Pharmakokinetik mit sehr geringer Clearance (Cl: 0,02 L kg-1 h-1) und geringem Verteilungsvolumen (Vdss: 0,2 L kg-1). Darüber hinaus zeigt diese Verbindung auch eine moderate Halbwertszeit (T1/2: 5,8 Stunden) und eine gute orale Bioverfügbarkeit (F: 58 %). In den Kaninchenmodellen für arteriovenöse Shunt-Thrombose (AVST), venöse Thrombose (VT) und elektrisch vermittelte Halsschlagaderthrombose (ECAT) erzeugt es dosisabhängige antithrombotische Effekte mit EC50 von 270 nM, 110 nM bzw. 70 nM. Diese Chemikalie hemmt die Factor Xa-Aktivität signifikant mit einer IC50 von 0,22 μM im Kaninchen ex vivo. Beim Schimpansen zeigt es auch ein kleines Verteilungsvolumen (Vdss: 0,17 L kg-1), eine geringe systemische Clearance (Cl: 0,018 L kg-1 h-1) und eine gute orale Bioverfügbarkeit (F: 59 %). |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06388239 | Not yet recruiting | Healthy Volunteer |
International Bio service |
August 26 2024 | Phase 1 |
| NCT05869591 | Recruiting | Liver Cirrhosis |
Centre Hospitalier Universitaire Vaudois |
January 18 2024 | Phase 2 |
| NCT05683808 | Not yet recruiting | Glioblastoma|Astrocytoma|Venous Thromboembolism |
University of Vermont Medical Center|Dartmouth-Hitchcock Medical Center|MaineHealth |
January 16 2023 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
