nur für Forschungszwecke
Domperidone Dopamine Receptor Inhibitor
Kat.-Nr.S2461
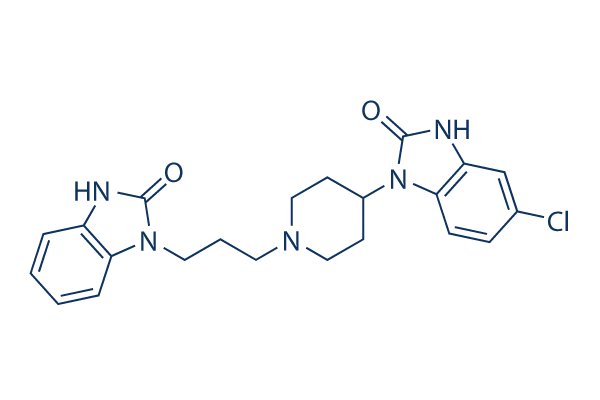
Chemische Struktur
Molekulargewicht: 425.91
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Dopamine Receptor Inhibitoren | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Rotundine Azaperone SKF38393 HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 425.91 | Formel | C22H24ClN5O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 57808-66-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CN(CCC1N2C3=C(C=C(C=C3)Cl)NC2=O)CCCN4C5=CC=CC=C5NC4=O | ||
Löslichkeit
|
In vitro |
DMSO
: 48 mg/mL
(112.69 mM)
Ethanol : 1 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Dopamine D2 receptor
|
|---|---|
| In vitro |
Domperidone (ein D2R-Antagonist) hemmt die Equilibrative NT1 (ENT1)-Aktivität in Gegenwart von Bromocriptin stärker als in Abwesenheit davon und weist in Madin-Darby-Rinder-Nierenzellen (MDBK) einen IC50-Wert auf, der niedriger ist als der von Bromocriptin oder Ergovalin.
|
| In vivo |
Domperidone (0,1 mg/kg) führt zu einer signifikanten Abnahme des Fressverhaltens und einer Stimulation des Grundstoffwechsels, hat aber keinen Einfluss auf die Lokomotorik von Ratten in einem Phenomaster-System. Diese Verbindung (1,1 mg/kg und 5,5 mg/kg, oral) erhöht den laminaren mikrovaskulären Blutfluss (LMBF) bei Pferden im Vergleich zu den Ausgangswerten signifikant, beginnend 4 Stunden nach der Verabreichung, und dieser Effekt hielt mindestens 8 Stunden an. Es (0,2 mg/kg, i.v.) erhöht den laminaren mikrovaskulären Blutfluss (LMBF) bei Pferden im Vergleich zu den Ausgangswerten 10 und 12 Stunden nach der Verabreichung signifikant. Diese Chemikalie kann schädliche reproduktive Effekte verbessern und die mit Fescue-Toxikose verbundenen Gewichtszunahme bei Färsen reduzieren. Domperidone-behandelte Stuten hatten eine kürzere Trächtigkeitsdauer und fohlten näher an ihrem erwarteten Geburtstermin als Kontrollstuten. Sie hatten höhere Brustdrüsenwerte und Serumprolaktinkonzentrationen. Es (5 mg/kg, oral) erhöht die Spitzenplasmakonzentration und die Fläche unter der Kurve von Paracetamol bei Ratten, was auf eine erhöhte Magenentleerung hindeutet. Diese Verbindung verringert die Dopamin-induzierte kontraktile Aktivität von Längsmuskelstreifen des mittleren Jejunums bei Ratten.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05570292 | Completed | Gastric Residual Volume |
Ain Shams University |
October 10 2022 | Phase 3 |
| NCT04653584 | Terminated | Parkinson Disease |
Assistance Publique - Hôpitaux de Paris |
January 1 2021 | -- |
| NCT03837067 | Completed | Parkinson''s Disease |
Assistance Publique - Hôpitaux de Paris |
July 17 2018 | -- |
| NCT01710462 | Withdrawn | Gastroesophageal Reflux Disease |
Eurofarma Laboratorios S.A. |
August 2013 | Phase 3 |
| NCT01907633 | Completed | Death Sudden Cardiac |
Janssen Research & Development LLC |
December 2011 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
