nur für Forschungszwecke
MPTP Hydrochloride Dopaminerges Neurotoxin
Kat.-Nr.S4732
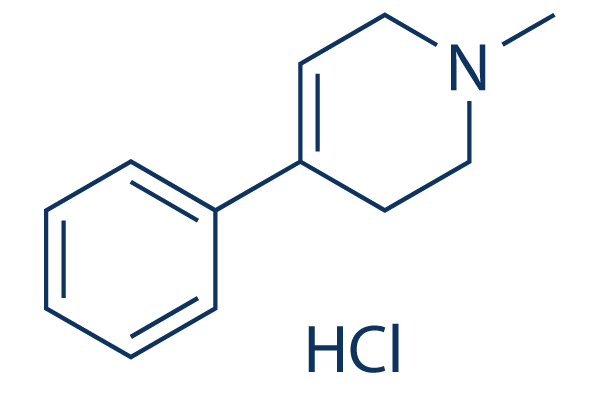
Chemische Struktur
Molekulargewicht: 209.72
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Dopamine Receptor Inhibitoren | Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone SKF38393 HCl |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| insect cells | Function assay | 120 mins | Inhibition of human recombinant MAOA expressed in insect cells assessed as oxidation of kynuramine substrate at 50 uM measured after additional enzyme added after 120 mins incubation | 22078410 | ||
| insect cells | Function assay | 90 mins | Inhibition of human recombinant MAOA expressed in insect cells assessed as oxidation of kynuramine substrate at 50 uM measured after additional substrate added after 90 mins incubation | 22078410 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 209.72 | Formel | C12H15N·HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 23007-85-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN1CCC(=CC1)C2=CC=CC=C2.Cl | ||
Löslichkeit
|
In vitro |
Water : 41 mg/mL Ethanol : 41 mg/mL
DMSO
: 26 mg/mL
(123.97 mM)
|
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Die Morphologie von N2AB-1- und Gliomzellen wurde nicht verändert, wenn diese Zellen allen Dosen von MPTP Hydrochloride ausgesetzt wurden. Und die Proliferation von C6-Gliomzellen wurde durch die Behandlung mit dieser Verbindung ebenfalls nicht beeinflusst. MPTP Promotes Apoptosis and Tau Phosphorylation in Human Neuroblastoma M17 Cells. Diese Verbindung fördert signifikant die Tau-Phosphorylierung an Ser262 in menschlichen Neuroblastom-M17-Zellen. Sie verursachte eine dosisabhängige Zunahme des intrazellulären α-Synuclein-Spiegels in unseren M17-Human-Neuroblastom-Zellen. Diese Chemikalie scheint die Tau-Phosphorylierung im Gehirn durch Aktivierung von PKA und GSK3β zu fördern.
|
|---|---|
| In vivo |
Die Anzahl der Tyrosinhydroxylase-positiven Neuronen war in der Substantia nigra pars compacta von MPTP-behandelten Mäusen verringert. Diese Verbindung verringerte die Expression von Thioredoxinreduktase 1 und die Thioredoxinreduktase-Aktivität im Maus-Mittelhirn, reduzierte die Anzahl der Thioredoxinreduktase 1-positiven Zellen in der Substantia nigra pars compacta von Mäusen. Die Verabreichung dieses Toxins kann neurochemische, verhaltensbezogene und histopathologische Veränderungen bei Menschen und nicht-menschlichen Primaten verursachen, die denen ähneln, die bei Parkinson-Patienten beobachtet werden. Im Vergleich zu Primaten sind Nagetiere unempfindlich gegenüber MPTP. Diese Chemikalie kann über verschiedene Wege verabreicht werden, wie z. B. Magensonde und stereotaktische Injektion, aber der gebräuchlichste und reproduzierbarste Weg ist die systemische Verabreichung, einschließlich subkutaner, intravenöser, intraperitonealer und intramuskulärer Injektion. Es ist ein lipophiles Protoxin, das nach systemischer Injektion schnell die Blut-Hirn-Schranke überwinden kann. Sobald es in das Gehirn gelangt, wird MPTP durch Monoaminoxidase B in 1-Methyl-4-phenylpyridin umgewandelt. Es hat sich gezeigt, dass es für dopaminerge Neuronen des nigrostriatalen Systems bei Menschen, Affen und Mäusen toxisch ist und eine langanhaltende Depletion von DA und seinen Metaboliten im Striatum hervorruft.
|
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | TH / Actin pCaMKIIβ / pCaMKIIα / CaMKIIβ / CaMKIIα / β-Actin TH / p-α-Syn / α-Syn / β-actin / CDK5 / LC3-I / LC3-II / p62 / NLRP3 / ASC / Casp1 p20 / Procasp1 p-ERK1/2 / ERK1/2 / GAPDH GDH2 / GDH1 / GFAP / GAPDH |

|
23391753 |
| IHC | tyrosine hydroxylase (TH) tyrosine hydroxylase (TH) SNpc tyrosine hydroxylase (TH) Substantia nigra |
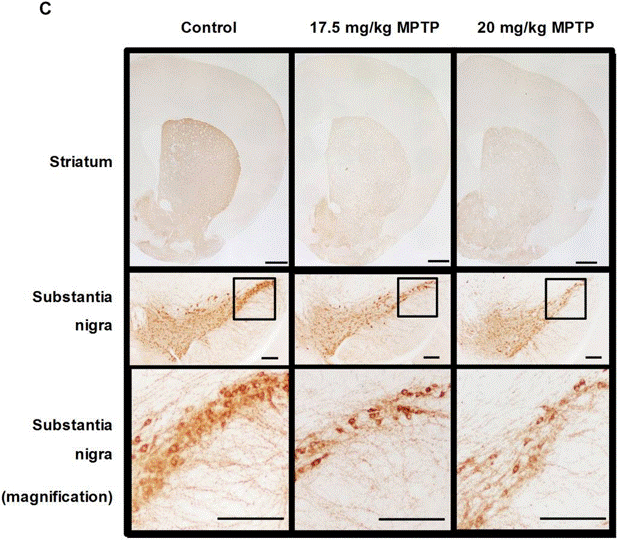
|
31427934 |
| Immunofluorescence | tyrosine hydroxylase (TH) / miR-188-3p α-Syn tyrosine hydroxylase (TH) / Tunel tyrosine hydroxylase (TH) / Tunel tyrosine hydroxylase (TH) GFAP |
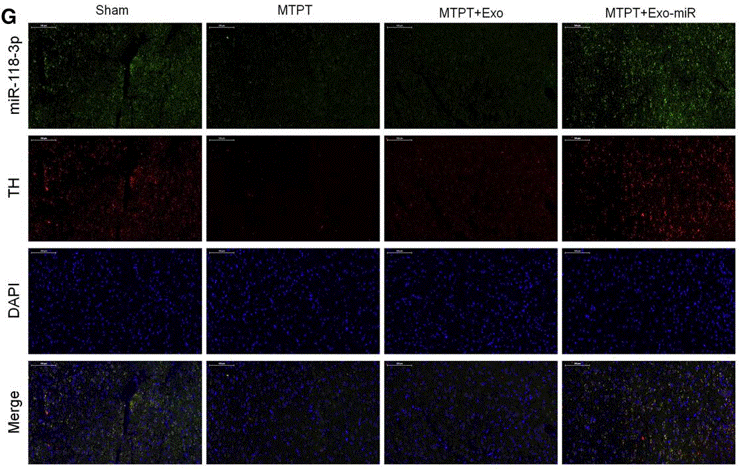
|
33717653 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
