nur für Forschungszwecke
Quetiapine (ICI-204636) fumarate Dopamine Receptor Antagonist
Kat.-Nr.S1763
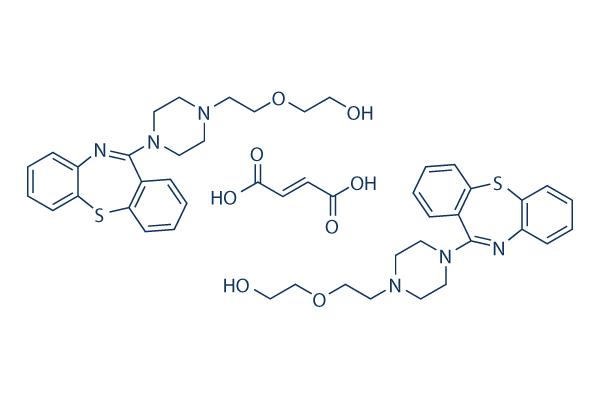
Chemische Struktur
Molekulargewicht: 883.09
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Dopamine Receptor Inhibitoren | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 883.09 | Formel | C46H54N6O8S2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 111974-72-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | ICI-204636 fumarate | Smiles | C1CN(CCN1CCOCCO)C2=NC3=CC=CC=C3SC4=CC=CC=C42.C1CN(CCN1CCOCCO)C2=NC3=CC=CC=C3SC4=CC=CC=C42.C(=CC(=O)O)C(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 36 mg/mL
(40.76 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Dopamine receptor
Histamine receptor
Adrenergic Receptor
|
|---|---|
| In vitro |
Quetiapine zeigt Affinität zu verschiedenen Neurotransmitterrezeptoren, einschließlich Serotonin, Dopamin, Histamin und adrenergen Rezeptoren, und weist Bindungseigenschaften am Dopamin-2-Rezeptor auf, die denen von Clozapin ähneln.
|
| In vivo |
Quetiapine hat ein präklinisches Profil, das auf eine antipsychotische Aktivität mit einer reduzierten Neigung zu extrapyramidalen Symptomen (EPS) und einer anhaltenden Prolaktinerhöhung hindeutet. Guetiapin verändert die Neurotensin-Neurotransmission und die c-fos-Expression in limbischen, aber nicht motorischen Gehirnbereichen. Quetiapine zeigt auch Clozapin-ähnliche Aktivität in einer Reihe von Verhaltens- und biochemischen Tests und kann neuroprotektive Eigenschaften besitzen. Quetiapine verhindert dosisabhängig Schizophrenie und Depression bei der hippokampalen Zellproliferation und BDNF-Expression, die durch chronischen Stress (CRS) bei Ratten verursacht werden. Guetiapin (5 mg/kg) in Kombination mit Venlafaxin (2,5 mg/kg) erhöht die hippokampale Zellproliferation und verhindert den BDNF-Abfall bei gestressten Ratten, während jedes der Medikamente milde oder keine Wirkungen zeigt. Guetiapin erzeugt selektive Effekte auf kortikale und limbische Regionen des Gehirns und insbesondere auf die dopaminerge Neurotransmission in diesen Regionen. Guetiapin erzeugt geringere Werte der putaminalen DA D2r-Besetzung als die für typische APDs berichteten. Quetiapine erzeugt auch eine bevorzugte Besetzung des temporalen kortikalen DA D2r von 46,9 %, verschont aber nicht die Besetzung der Substantia nigra DA D2r. Guetiapin schwächt den Rückgang des Spiegels des hirnbestimmten neurotrophen Faktors (BDNF) in den Hippocampi von Ratten ab, die chronischem Stress ausgesetzt waren. Guetiapin (10 mg/kg) kehrt die stressinduzierte Unterdrückung der hippokampalen Neurogenese um, was sich in den Zahlen der BrdU-markierten und pCREB-positiven Zellen zeigt, die mit denen in nicht gestressten Ratten vergleichbar, aber höher sind als die in Vehikel-behandelten Ratten.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00837343 | Unknown status | Bipolar Disorder |
Guangzhou Mental Hospital|First Affiliated Hospital of Jinan University|Second Affiliated Hospital of Guangzhou Medical University|Guangzhou mental Hospital Attached to Guangzhou Civil Affairs Bureau |
December 2008 | Phase 4 |
| NCT00838032 | Unknown status | Acute Schizophrenia |
Sichuan University |
August 2008 | Phase 4 |
| NCT00631722 | Completed | Schizophrenia |
Peking University |
May 2007 | Not Applicable |
| NCT00448578 | Completed | Mania|Bipolar Disorder |
AstraZeneca |
August 2005 | Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
I want to know if your recommended formulation for in vivo experiments on the website is suitable for oral administration or injection?
Antwort:
It can be dissolved in 0.5% CMC Na at 30 mg/ml as a suspension and is fine for oral gavage.
