nur für Forschungszwecke
Ranitidine Hydrochloride Histamine Receptor Antagonist
Kat.-Nr.S1801
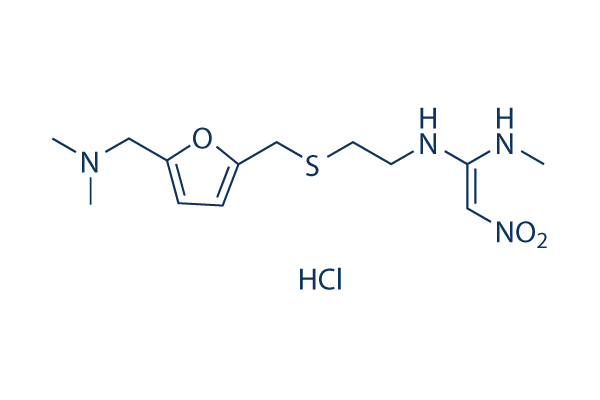
Chemische Struktur
Molekulargewicht: 350.86
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Histamine Receptor Inhibitoren | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Betahistine 2HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 350.86 | Formel | C13H22N4O3S.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 66357-59-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | AH19065 | Smiles | CNC(=C[N+](=O)[O-])NCCSCC1=CC=C(O1)CN(C)C.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 70 mg/mL
(199.5 mM)
Water : 70 mg/mL Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Histamine H2 receptor
|
|---|---|
| In vitro |
Ranitidine sensibilisiert Hepatozyten für die Zerstörung durch zytotoxische Produkte aus aktivierten Neutrophilen, während Famotidin diese Fähigkeit nicht besitzt. Ranitidine hemmt die Produktion von Tumornekrosefaktor-alpha (TNF-alpha) in Monozyten, die in vitro mit Lipopolysaccharid stimuliert wurden. Ranitidine reduziert dosisabhängig den Kel von Morphin mit einem Maximaleffekt von 50 % und erhöht die relative Konzentration von Morphin-6-Glucuronid zu Morphin-3-Glucuronid in isolierten Meerschweinchen-Hepatozyten. Ranitidine senkt das Morphin-3-Glucuronid/Morphin-6-Glucuronid-Verhältnis schrittweise um bis zu 21 %.
|
| In vivo |
Ranitidine führt zu Leberschäden, was durch erhöhte Serum-Alanin-Aminotransferase-, Aspartat-Aminotransferase- und Gamma-Glutamyl-Transferase-Aktivitäten innerhalb von 6 Stunden nach Ranitidine-Verabreichung bei Ratten belegt wird. Ranitidine hemmt den durch hepatische Ischämie/Reperfusion induzierten Anstieg der hepatischen Gewebespiegel von TNF-alpha, des Zytokin-induzierten Neutrophilen-Chemoattraktans und der hepatischen Akkumulation von Neutrophilen bei Ratten. Eine Ranitidine-Begleitbehandlung verstärkt die LPS-induzierte Gerinnung vor Leberschäden, und Antikoagulanzien reduzieren Leberschäden bei LPS/RAN-behandelten Ratten. Ranitidine/LPS-behandelte Ratten führen zur Bildung von Fibrin-Gerinnseln in Lebersinusoiden, und die Prävention der Fibrinablagerung ist mit einer reduzierten hepatozellulären Schädigung verbunden. Eine Ranitidine-Begleitbehandlung verstärkt den LPS-induzierten TNF-Anstieg vor dem Einsetzen der hepatozellulären Schädigung bei Ratten. Ranitidine zeigt anxiolytische Effekte im erhöhten Plus-Labyrinth, was durch eine erhöhte Verweildauer in den offenen Armen, mehr Abtasten der offenen Arme und mehr Endexkursionen bei Ratten angezeigt wird.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05399927 | Completed | Music Therapy|Cardiovascular Diseases|Critical Care|Emergencies |
Universidad Miguel Hernandez de Elche |
July 2015 | Not Applicable |
| NCT01539655 | Completed | Medullary Thyroid Cancer |
Sanofi |
February 2012 | Phase 1 |
| NCT01017198 | Completed | Advanced Solid Tumors |
Biogen |
November 2009 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
