nur für Forschungszwecke
Rivaroxaban Factor Xa Inhibitor
Kat.-Nr.S3002
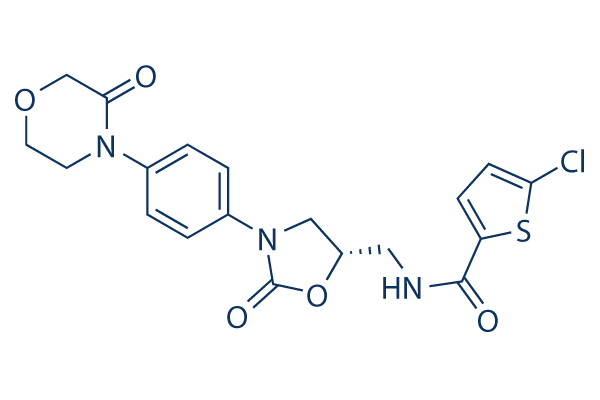
Chemische Struktur
Molekulargewicht: 435.88
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere Factor Xa Inhibitoren | Asundexian |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 435.88 | Formel | C19H18ClN3O5S |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 366789-02-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | BAY 59-7939 | Smiles | C1COCC(=O)N1C2=CC=C(C=C2)N3CC(OC3=O)CNC(=O)C4=CC=C(S4)Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 87 mg/mL
(199.59 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Factor Xa
(Cell-free assay) 0.7 nM
Prothrombinase
(Cell-free assay) 2.1 nM
|
|---|---|
| In vitro |
Rivaroxaban ist ein oraler, direkter Inhibitor von Factor Xa (FXa), der zur Prävention und Behandlung von arteriellen und venösen Thrombosen mit einem Ki von 0,4 nM entwickelt wird. Diese Verbindung hemmt auch die Prothrombinase-Aktivität mit einer IC50 von 2,1 nM. Sie zeigt auch eine ähnliche Affinität zu gereinigtem menschlichem und kaninchem FXa (IC50 0,7 nM bzw. 0,8 nM), aber eine geringere Potenz gegen gereinigtes Ratten-FXa (IC50 3,4 nM). Endogenes menschliches und kanisches FXa im Plasma wird durch diese Chemikalie in ähnlichem Maße gehemmt (IC50 21 nM bzw. 21 nM), während im Rattenplasma 14-fach höhere Konzentrationen erforderlich sind (IC50 290 nM). Es zeigt eine hohe Permeabilität und einen polarisierten Transport durch Caco-2-Zellen als Substrat des P-gp, zeigt aber keine hemmende Wirkung auf den P-gp-vermittelten Medikamententransport bis zu Konzentrationen von 100 μM in vitro.
|
| Kinase-Assay |
Factor Xa Aktivität
|
|
Die Aktivität von Rivaroxaban gegen gereinigte Serinproteasen wird unter Verwendung chromogener oder fluorogener Substrate in 96-Well-Mikrotiterplatten gemessen. Die Enzyme werden 10 Minuten lang mit dieser Verbindung oder ihrem Lösungsmittel, Dimethylsulfoxid (DMSO), inkubiert. Die Reaktionen werden durch Zugabe des Substrats gestartet, und die Farbe oder Fluoreszenz wird kontinuierlich bei 405 nm mit einem Spectra Rainbow Thermo Reader oder bei 630/465 nm mit einem SPECTRAfluor plus für 20 Minuten überwacht. Die enzymatische Aktivität wird in den folgenden Puffern (Endkonzentrationen) analysiert: menschliches FXa (0,5 nM), kanisches FXa (2 nM), Ratten-FXa (10 nM) oder Urokinase (4 nM) in 50 mM Tris–HCl-Puffer pH 8,3, 150 mM NaCl und 0,1 % Rinderserumalbumin (BSA); Pefachrom FXa (50–800 μM) oder Chromozym U (250 μM) mit Thrombin (0,69 nM), Trypsin (2,2 nM) oder Plasmin (3,2 nM) in 0,1 μM Tris–HCl, pH 8,0 und 20 mM CaCl2; Chromozym TH (200 μM), Chromozym Plasmin (500 μM) oder Chromozym Trypsin (500 μM) mit FXIa (1 nM) oder APC (10 nM) in 50 mM Phosphatpuffer, pH 7,4, 150 mM NaCl; und S 2366 (150 oder 500 μM) mit FVIIa (1 nM) und Gewebefaktor (3 nM) in 50 mM Tris–HCl-Puffer, pH 8,0, 100 mM NaCl, 5 mM CaCl2 und 0,3 % BSA, H-D-Phe-Pro-Arg-6-amino-1-naphthalen-benzylsulfonamid-H2O (100 μM) und 3 Stunden lang gemessen. Der FIXaβ/FX-Assay, bestehend aus FIXaβ (8,8 nM) und FX (9,5 nM) in 50 mM Tris–HCl-Puffer, pH 7,4, 100 mM NaCl, 5 mM CaCl2 und 0,1 % BSA, wird durch Zugabe von I-1100 (50 μM) gestartet und 60 Minuten lang gemessen. Die Hemmkonstante (Ki) gegen FXa wird nach der Cheng–Prusoff-Gleichung berechnet. Die IC50 ist die Menge des Inhibitors, die erforderlich ist, um die Anfangsgeschwindigkeit der Kontrolle um 50 % zu verringern.
|
|
| In vivo |
Rivaroxaban reduziert venöse Thrombosen dosisabhängig (ED50 0,1 mg/kg i.v.) in einem Ratten-Venenthrombosemodell. Diese Verbindung reduziert die arterielle Thrombusbildung in einem arteriovenösen (AV) Shunt bei Ratten (ED50 5,0 mg/kg p.o.) und Kaninchen (ED50 0,6 mg/kg p.o.). Die Plasmakinetik dieser Chemikalie ist im untersuchten Dosisbereich linear (1-10 mg/kg bei Ratten, 0,3-3 mg/kg bei Hunden). Die Plasmaclearance ist gering: 0,4 L/kg/h bei Ratten und 0,3 L/kg/h bei Hunden; das Verteilungsvolumen (V(ss)) ist moderat: 0,3 L/kg bei Ratten und 0,4 L/kg bei Hunden. Die Eliminationshalbwertszeit nach oraler Verabreichung ist bei beiden Spezies kurz (0,9-2,3 Stunden).
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06193863 | Not yet recruiting | Prevention of Venous Thromboembolism|Congenital Heart Disease|Fontan Procedure|Children |
Bayer|Janssen Research & Development LLC |
May 31 2024 | -- |
| NCT06195540 | Not yet recruiting | Venous Thromboembolism|Deep Vein Thrombosis|Pulmonary Embolism|Lower Limb Trauma|Thromboprophylaxis|Immobilisation |
University Hospital Angers |
May 31 2024 | Phase 3 |
| NCT06314763 | Completed | Drug Drug Interaction Study |
Radboud University Medical Center|Amgen |
November 9 2023 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
