nur für Forschungszwecke
S 38093 Histamine Receptor Antagonist
Kat.-Nr.S8598
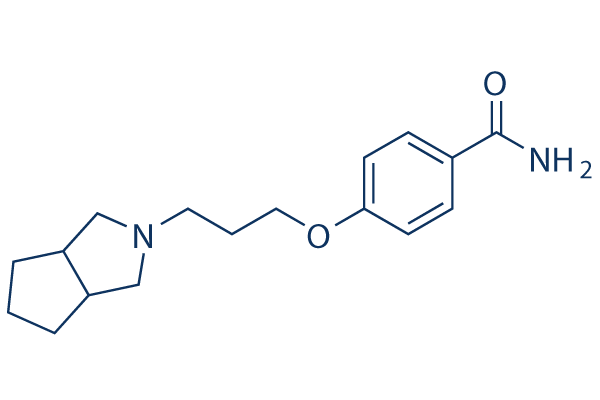
Chemische Struktur
Molekulargewicht: 288.38
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Histamine Receptor Inhibitoren | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Betahistine 2HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 288.38 | Formel | C17H24N2O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 862896-30-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CC2CN(CC2C1)CCCOC3=CC=C(C=C3)C(=O)N | ||
Löslichkeit
|
In vitro |
DMSO
: 57 mg/mL
(197.65 mM)
Ethanol : 57 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
human H3 receptor
1.2 μM(Ki)
mouse H3 receptor
1.44 μM(Ki)
rat H3 receptor
8.8 μM(Ki)
|
|---|---|
| In vitro |
In zellulären Modellen konnte diese Verbindung Mäuse-H3-Rezeptoren antagonisieren (KB = 0,65 μM) und die durch einen H3-Agonisten induzierte cAMP-Abnahme über menschliche H3-Rezeptoren unterdrücken (KB = 0,11 μM). Unter den vier histaminergen Rezeptor-Subtypen ist sie selektiv für den H3-Rezeptor, wobei ihre Bindungsaffinität für H1-, H2- und H4-Rezeptoren vernachlässigbar ist.
|
| In vivo |
S 38093, ein neuartiger hirngängiger Antagonist/inverser Agonist von H3-Rezeptoren, auf AHN (Proliferation, Reifung und Überleben) bei 3 Monate alten und bei 16 Monate alten Mäusen. Bei gealterten Tieren induzierte diese Verbindung eine Umkehrung altersabhängiger Effekte auf hippokampale Hirn-abgeleiteter neurotropher Faktor (BDNF) BDNF-IX, BDNF-IV und BDNF-I Transkripte und erhöhte die Expression des vaskulären endothelialen Wachstumsfaktors (VEGF). Die Effekte einer chronischen Verabreichung dieser Verbindung wurden in einem neurogenese-abhängigen „Kontextdiskriminierungstest (CS)“ bei gealterten Mäusen bewertet. Während das Altern die Maus-CS veränderte, verbesserte die chronische Behandlung mit dieser Chemikalie die CS signifikant. Eine chronische Behandlung mit dieser Verbindung erhöht die adulte hippocampale Neurogenese und könnte eine innovative Strategie zur Verbesserung altersassoziierter kognitiver Defizite bieten. Diese Verbindung erweist sich als wirksam in einer mittleren pharmakologischen Dosis von 0,3–1 mg/kg p.o./i.p. in Tierverhaltens-Tests des Arbeitsgedächtnisses (Morris-Wasserlabyrinth bei Ratten; spontane Alternation und gleichzeitige serielle Alternationstests bei Mäusen; verzögertes Matching nach Probe bei gealterten Affen) und des episodischen Gedächtnisses (soziale und Objekterkennungstests bei Ratten; kontextuelle Diskriminierungsaufgabe bei Mäusen). Es verbessert auch Aufmerksamkeit, exekutive Funktionen und kognitive Flexibilität bei MPTP-behandelten Affen. Darüber hinaus, im Einklang mit seinen H3-Antagonisten/inversen Agonisten-Eigenschaften, erhöht diese Chemikalie dosisabhängig die extrazellulären Histaminspiegel im präfrontalen Kortex und erleichtert die cholinerge Transmission im präfrontalen Kortex und Hippocampus von Ratten nach sowohl akuter als auch chronischer Verabreichung. Diese Verbindung wurde bei Maus und Ratte schnell (Tmax = 0,25-0,5h), bei Affen langsam (2h) resorbiert, mit einer Bioverfügbarkeit von 20 bis 60% und einer t1/2 von 1,5h bis 7,4h. Die Verbindung wurde weit verbreitet mit einem moderaten Verteilungsvolumen und geringer Proteinbindung. Die Hirnverteilung dieser Chemikalie war schnell und hoch.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
