nur für Forschungszwecke
Histamine 2HCl Histamine Receptor Agonist
Kat.-Nr.S4118
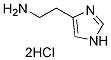
Chemische Struktur
Molekulargewicht: 184.07
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Histamine Receptor Inhibitoren | GSK2879552 Dihydrochloride JNJ-7777120 Ebastine Ciproxifan Maleate Mianserin HCl Astemizole Lafutidine Mizolastine Rupatadine Fumarate Betahistine 2HCl |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 184.07 | Formel | C5H9N3.2HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 56-92-8 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Ceplene | Smiles | C1=C(NC=N1)CCN.Cl.Cl | ||
Löslichkeit
|
In vitro |
Water : 37 mg/mL
DMSO
: 3 mg/mL
(16.29 mM)
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Histamine H1 receptor
Histamine H2 receptor
|
|---|---|
| In vitro |
Histamine unterdrückt die Bildung von ROS über den Histamine-Typ-2-Rezeptor (H2-Rezeptor). Histamine hemmt die Bildung und Freisetzung reaktiver Sauerstoffspezies (ROS) durch Monozyten/Makrophagen (MO) während des respiratorischen Bursts. Histamine und Interleukin-2 (IL-2) wirken synergistisch, um die NK-Zellzytotoxizität (NKCC) zu aktivieren. Histamine in Kombination mit IL-2 könnte die Ansprechraten und das krankheitsfreie Überleben verbessern, indem es die Zellen des Immunsystems vor oxidativem Stress schützt und die natürliche endogene Immunozytotoxizität induziert. |
| In vivo |
Histamine-Behandlung (0,5 mg/kg oder 5,0 mg/kg, zweimal täglich) schützt vor Leberschäden, was sich in normalen Serumtransaminasespiegeln und signifikant reduzierten Leberpathologiewerten in einem Rattenmodell mit früher alkoholinduzierter Leberschädigung zeigt. Die schützende Wirkung von Histamine wird durch Ranitidin (10 mg/kg), einen H2-Rezeptorantagonisten, blockiert, was darauf hindeutet, dass die Histamine-Wirkung überwiegend über den H2-Rezeptor vermittelt wird. Histamine (30 pg/Ratte, icv) erhöht sowohl die 3,4-Dihydroxyphenylalanin-Akkumulation als auch die 3,4-Dihydroxyphenylalanin-Säurekonzentrationen im Nucleus accumbens bei männlichen Ratten, und dieser Effekt wird nicht durch den H2-Antagonisten Zolantidin beeinflusst, was darauf hindeutet, dass Histamine mesolimbische DA-Neuronen durch eine Wirkung am H1-Rezeptor stimuliert. Histamine (0,5 mg/kg s.c.) reduziert das Lebertumorgewicht um 46 % und das subkutane Tumorgewicht um 41 % im Vergleich zu Ratten, die subkutane Kochsalzinjektionen erhalten. Die durch subkutane Histamine-Injektionen beobachtete Antitumorwirkung wird durch Ranitidin (50 mg/kg s.c.) im Rattensarkom gehemmt. Histamine (1000 mg/kg s.c.) zeigt nach 24 Stunden akute Gewebeschäden und Anzeichen einer pathologischen Entzündung an den Injektionsstellen nach 5 und 28 Tagen bei Sprague-Dawley-Ratten. Histamine (1000 mg/kg s.c.) führt zu einer Cmax von 167 mM, einer tmax von 0,5 Stunden, einer t1/2 von 0,95 und einer AUC von 186 mmol-h/L bei männlichen Sprague-Dawley-Ratten. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06281366 | Recruiting | Pregnancy Complications |
Hospital Universitari Vall d''Hebron Research Institute|DR Healthcare |
February 16 2024 | -- |
| NCT05216133 | Enrolling by invitation | Airway Disease|Barrett Esophagus|Gastroesophageal Reflux Disease |
NYU Langone Health|National Institute for Occupational Safety and Health (NIOSH/CDC) |
March 22 2023 | -- |
| NCT05701826 | Completed | Skeletal Muscle Relaxation |
Fujian Shengdi Pharmaceutical Co. Ltd. |
February 15 2023 | Phase 1 |
| NCT05676346 | Completed | Lower Urinary Tract Symptoms|Histamine Intolerance |
Complexo Hospitalario Universitario de A Coruña |
October 11 2022 | -- |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
