nur für Forschungszwecke
Hygromycin B Antibiotikum
Kat.-Nr.S2908
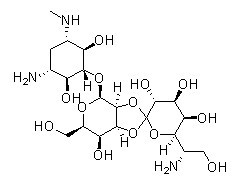
Chemische Struktur
Molekulargewicht: 527.52
Qualitätskontrolle
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
- Zitiert in Nature Medicine für seine erstklassige Qualität
- COA
- NMR
- Datenblatt
- SDS
| Verwandte Ziele | Integrase Bacterial Antibiotics Anti-infection Fungal Antiviral COVID-19 Parasite Reverse Transcriptase HIV |
|---|---|
| Weitere Antineoplastic and Immunosuppressive Antibiotics Inhibitoren | Staurosporine (STS) Cyclosporin A Oligomycin A (MCH 32) Puromycin Dihydrochloride Nigericin sodium salt Geldanamycin (NSC 122750) Honokiol Streptozotocin (STZ) Sodium Monensin (NSC 343257) Cephalomannine |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 527.52 | Formel | C20H37N3O13 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 31282-04-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Hygrovetine | Smiles | CNC1CC(C(C(C1O)OC2C3C(C(C(O2)CO)O)OC4(O3)C(C(C(C(O4)C(CO)N)O)O)O)O)N | ||
Löslichkeit
|
In vitro |
Water : 100 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| In vitro |
Hygromycin B hat eine einzige Bindungsstelle innerhalb des 30S, sie befindet sich in der großen Furche der Helix sehr nahe an der helikalen Achse und stellt Kontakt mit Nukleotiden beider RNA-Stränge in den Regionen 1490-1500 und 1400–1410 her. Ring I von HygB ist an nicht-sequenzspezifischen Wechselwirkungen mit den Phosphat-Sauerstoffatomen des Rückgrats von G1494 beteiligt, zusätzlich zu basenspezifischen Wechselwirkungen mit G1494 und U1495. Ringe II und III bilden schwache basenspezifische Wasserstoffbrücken zu C1404 und U1498, aber ihre Hauptrolle besteht anscheinend darin, Ring IV für die Wechselwirkung mit Basen in der Region 1496–1498 zu positionieren. Ring IV von HygB kommt innerhalb von 4 Å der zweiten Base des an der P-Stelle gebundenen mRNA-Codons. Diese Verbindung (0,38 mM) stoppt das Wachstum von Hefezellen in reichhaltigen Medien vollständig. Sie blockiert die Polypeptidsynthese in zellfreien Extrakten aus Kaninchenretikulozyten, Weizenkeimen und Hefe stark. Sie hemmt die Peptidkettenverlängerung durch Hefe-Polysomen, indem sie die Elongationsfaktor-EF-2-abhängige Translokation verhindert. Dieses Antibiotikum hemmt (80 %) die Elongationsfaktor-(EF)G-plus-GTP-abhängige Reaktion von entweder AcPhe-tRNA oder natürlicher Peptidyl-tRNA mit Puromycin in zellfreien Systemen von Escherichia coli. Es blockiert die nascenten Peptidketten entweder von gereinigten endogenen E. coli-Polysomen oder Poly(uridylsäure)-programmierten ribosomes während der Polypeptidsynthese. Es hemmt die nicht-enzymatische Translokation und die Freisetzung von AcPhe-tRNA von der ribosomalen Akzeptorstelle, die durch Depletion von NH4-Ionen gefördert wird. Es wird zur Resistenzselektion in Maus-L-Zellen verwendet, die mit Escherichia coli-Genen transfiziert wurden, die für die Resistenz gegen die Aminocyclitol-Antibiotika Hygromycin B kodieren. Diese Chemikalie wird als selektiver Marker für den T-DNA-Transfer und die Integration in den ektomykorrhizischen Pilz Suillus bovinus verwendet. |
Literatur |
|
|---|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
