nur für Forschungszwecke
LDN-193189 BMP-Signalweg-Inhibitor
Kat.-Nr.S2618
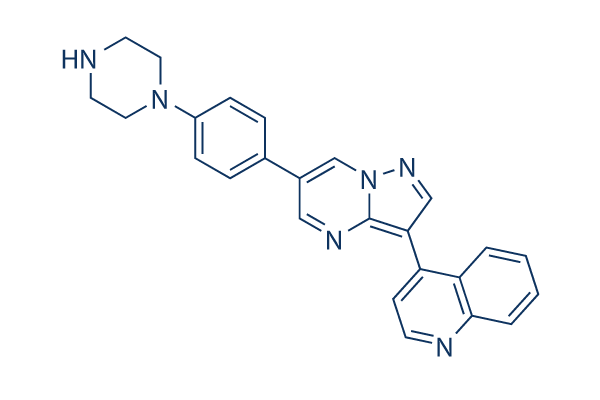
Chemische Struktur
Molekulargewicht: 406.48
Qualitätskontrolle
| Verwandte Ziele | PKC ROCK Bcr-Abl |
|---|---|
| Weitere TGF-beta/Smad Inhibitoren | SB431542 RepSox (E-616452) Vactosertib (TEW-7197) A-83-01 LDN-193189 Dihydrochloride Galunisertib (LY2157299) SRI-011381 (C381) LY2109761 SIS3 Hydrochloride SB-525334 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| C2C12 | Kinase Assay | inhibits the kinase activity of ALK4 and ActRIIA with IC50 values of 101 and 210 nm, respectively | 25368322 | |||
| EOC216 | Growth Inhibition Assay | 0.1-10 μM | 2-10 d | DMSO | induce cell death in a dose-dependent manner | 25227893 |
| OVAC429 | Growth Inhibition Assay | 2/5 μM | 48 h | DMSO | decreases the percentage of cells in S phas | 25227893 |
| SKOV3 | Growth Inhibition Assay | 2/5 μM | 48 h | DMSO | decreases the percentage of cells in S phas | 25227893 |
| OVCA429 | Growth Inhibition Assay | 2/5 μM | 48 h | DMSO | decreases the percentage of cells in S phas | 25227893 |
| EOC219 | Growth Inhibition Assay | 2/5 μM | 48 h | DMSO | decreases the percentage of cells in S phas | 25227893 |
| A549 | Growth Inhibition Assay | 0.5-16 μM | DMSO | inhibits cell growth in a dose-dependent manner | 24778011 | |
| BEAS-2B | Growth Inhibition Assay | 0.5-16 μM | DMSO | inhibits cell growth in a dose-dependent manner | 24778011 | |
| hBMSCs | Function Assay | 0.2 μM | 7 d | abolishes the silibinin-promoted ALP activity partly | 24076187 | |
| PANC-1 | Growth Inhibition Assay | 5-500 nM | 48 h | inhibits cell growth in a dose-dependent manner | 23969729 | |
| MIA PaCa-2 | Growth Inhibition Assay | 5-500 nM | 48 h | inhibits cell growth in a dose-dependent manner | 23969729 | |
| Bx-PC3 | Growth Inhibition Assay | 5-500 nM | 48 h | inhibits cell growth in a dose-dependent manner | 23969729 | |
| PC3 | Function Assay | 500 nM | 2 h | represses activation of Smad1/5/8 and P-Smad3 levels | 22452883 | |
| LNCaP | Function Assay | 0–500 nM | 2 h | reverses rapamycin-induced cell death | 22452883 | |
| EOC | Function Assay | 10-1000 nM | 72 h | reduces the phosphorylated BMP R-Smad1/5/8 | 22249415 | |
| HaCaT | Function Assay | 0.001-10 μM | 2 h | inhibits BMP2-induced phosphorylation of Smad1/5/8 with an IC50 of ~0.005 μM | 21740966 | |
| HaCaT | Function Assay | 0.001-10 μM | 2 h | inhibits the ability of ALK2 to phosphorylate GST-Smad1 with an IC50 of 45 nM | 21740966 | |
| HaCaT | Function Assay | 0.001-10 μM | 2 h | inhibits the ability of ALK3 to phosphorylate Smad1 with an IC50 of 100 nM | 21740966 | |
| HaCaT | Function Assay | 0.001-10 μM | 2 h | inhibits ALK4 and ALK5 with IC50 values of 0.3 μM and 0.5 μM respectively | 21740966 | |
| C2C12 | Function assay | 30 mins | Inhibition of BMP6-induced ALK2 transcriptional activity in mouse C2C12 cells expressing BRE-Luc after 30 mins by luciferase reporter gene assay, EC50 = 0.014 μM. | 30227946 | ||
| BT-12 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| fibroblast cell | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for control Hh wild type fibroblast cells | 29435139 | |||
| Rh30 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh30 cells | 29435139 | |||
| KB-3-1 | Function assay | P-glycoprotein substrates identified in KB-3-1 adenocarcinoma cell line, qHTS therapeutic library screen | 31515284 | |||
| C2C12 | Function assay | 0.1 uM | Inhibition of ALK5 in mouse C2C12 cells assessed as decrease in TGFbeta1-induced Smad1/5 phosphorylation at 0.1 uM by Western blot method | 28103025 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 406.48 | Formel | C25H22N6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1062368-24-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | DM3189 | Smiles | C1CN(CCN1)C2=CC=C(C=C2)C3=CN4C(=C(C=N4)C5=CC=NC6=CC=CC=C56)N=C3 | ||
Löslichkeit
|
In vitro |
0.01M HCl : 2.5 mg/mL
DMSO
: Insoluble
Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
ALK1
(Cell-free assay) 0.8 nM
ALK2
(Cell-free assay) 0.8 nM
ALK3
(Cell-free assay) 5.3 nM
ALK6
(Cell-free assay) 16.7 nM
|
|---|---|
| In vitro |
LDN-193189 hemmt potent die BMP4-vermittelte Smad1-, Smad5- und Smad8-Aktivierung mit einer IC50 von 5 nM und hemmt effizient die Transkriptionsaktivität der BMP-Typ-I-Rezeptoren ALK2 und ALK3 mit einer IC50 von 5 nM bzw. 30 nM. Darüber hinaus zeigt diese Verbindung auch eine hemmende Wirkung auf die Transkriptionsaktivität, die entweder durch konstitutiv aktive ALK2R206H- oder ALK2Q207D-Mutationsproteine induziert wird. Eine aktuelle Studie zeigt, dass diese Chemikalie die Produktion reaktiver Sauerstoffspezies blockiert, die durch oxidiertes LDL während der Atherogenese in menschlichen Endothelzellen der Aorta induziert werden. |
| Kinase-Assay |
Alkalische Phosphatase-Aktivität
|
|
C2C12-Zellen werden in 96-Well-Platten mit 2.000 Zellen pro Well in DMEM, ergänzt mit 2 % FBS, ausgesät. Die Wells werden in Vierfachbestimmung mit BMP-Liganden und LDN-193189 oder Vehikel behandelt. Die Zellen werden nach 6 Tagen Kultur in 50 μL Tris-gepufferter Salzlösung und 1 % Triton X-100 gesammelt. Die Lysate werden für 1 Stunde zu p-Nitro-Phenylphosphat-Reagenz in 96-Well-Platten gegeben und anschließend die alkalische Phosphatase-Aktivität (Absorption bei 405 nm) evaluiert. Die Zellviabilität und -quantität werden mit Cell Titer Aqueous One (Absorption bei 490 nm) gemessen, wobei replizierte Wells identisch zu denen für die alkalische Phosphatase-Messung behandelt werden.
|
|
| In vivo |
Bei transgenen Mäusen mit konditionaler caALK2 und Ad.Cre am postnatalen Tag 7 (P7) führt LDN-193189 (3 mg/kg i.p.) zu leichten Verkalkungen um die linke Tibia und Fibula, die erstmals am P13 sichtbar sind, und verhindert radiologische Läsionen am P15, ohne Gewichtsverlust oder Wachstumsverzögerung, spontane Frakturen, verminderte Knochendichte oder Verhaltensauffälligkeiten zu verursachen. Diese Verbindung dorsaliert Zebrafischembryonen, indem sie Signalwege hemmt, die durch das Knochenmorphogenetische Protein (BMP)6 induziert werden, ohne die vaskuläre Entwicklung zu beeinflussen. Bei PCa-118b-Tumor-tragenden Mäusen schwächt diese chemische Behandlung das Tumorwachstum ab und reduziert die Knochenbildung in den Tumoren. Bei LDL-Rezeptor-defizienten (LDLR-/-) Mäusen hemmt dieses Mittel die Entwicklung von Atheromen potent. Darüber hinaus zeigt es auch hemmende Wirkungen auf die damit verbundene vaskuläre Entzündung, osteogene Aktivität und Verkalkung. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pSMAD1 / pSMAD5 / pSMAD8 / SMAD1 / SMAD5 / SMAD8 / ID1 / SMAD4 / PARP / Cleaved PARP |

|
31098401 |
| Immunofluorescence | Tbx18 / Hcn4 |
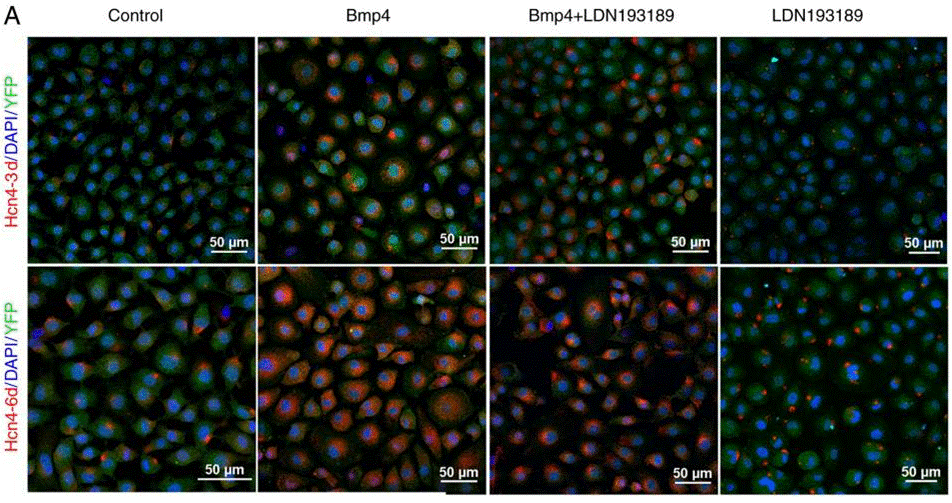
|
30906456 |
| Growth inhibition assay | Cell viability |
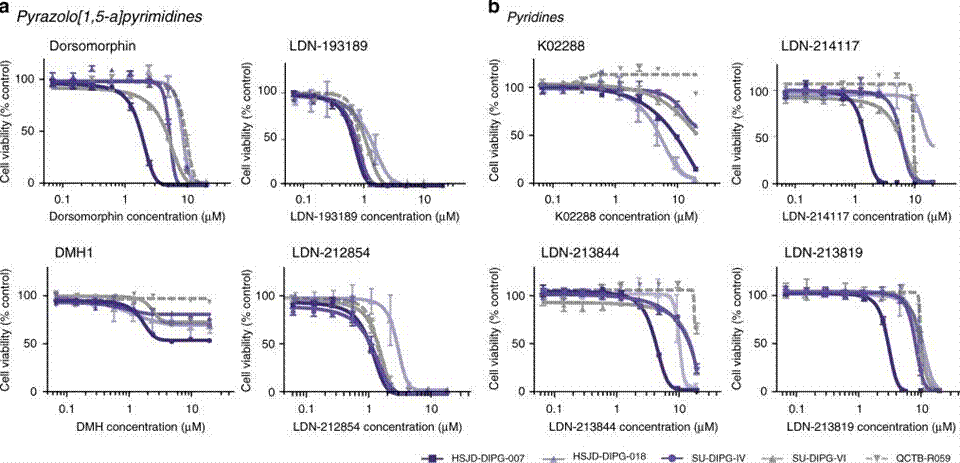
|
31098401 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
