nur für Forschungszwecke
LY2109761 TGF-beta/Smad Inhibitor
Kat.-Nr.S2704
Chemische Struktur
Molekulargewicht: 441.52
Qualitätskontrolle
Produkte, die oft zusammen verwendet werden mit LY2109761
| Verwandte Ziele | PKC ROCK Bcr-Abl |
|---|---|
| Weitere TGF-beta/Smad Inhibitoren | SB431542 RepSox (E-616452) Vactosertib (TEW-7197) LDN-193189 A-83-01 LDN-193189 Dihydrochloride SRI-011381 (C381) SIS3 Hydrochloride SB-525334 DMH1 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HepG2 | Function Assay | 10 μM | 2 h | inhibits autophagy induction by galangin | 25268046 | |
| PC-3 | Function Assay | 0.2/2/4 μM | 24 h | DMSO | inhibits TGF-β1–induced Smad2 activation | 22173053 |
| PMOs | Function Assay | 0.2/2/4 μM | 24 h | DMSO | inhibits TGF-β1–induced Smad2 activation | 22173053 |
| PC-3 | Growth Inhibition Assay | 0.2/2 μM | 24 h | DMSO | blocks the inhibition of cell proliferation produced by TGF-β1 | 22173053 |
| PMOs | Growth Inhibition Assay | 0.2/2 μM | 24 h | DMSO | blocks the inhibition of cell proliferation produced by TGF-β1 | 22173053 |
| U87MG | Growth Inhibition Assay | 5/10 μM | 2 h | enhances radiosensitivity | 22006998 | |
| T98 | Growth Inhibition Assay | 5/10 μM | 2 h | enhances radiosensitivity | 22006998 | |
| U87MG | Apoptosis Assay | 10 μM | 2 h | enhances radiation-induced DNA damage and apoptosis rates | 22006998 | |
| NMA-23 | Apoptosis Assay | 10 μM | 2 h | enhances radiation-induced DNA damage and apoptosis rates | 22006998 | |
| HLE | Function Assay | 0.01-100 nM | 48 h | inhibits the migration in a dose-dependent manner | 20844878 | |
| HLF | Function Assay | 0.01-100 nM | 48 h | inhibits the migration in a dose-dependent manner | 20844878 | |
| 10A/HER2YVMA | Growth Inhibition Assay | 0.1-0.5 μM | 9 d | reduces the size, invasiveness and cell number of colonies | 20383197 | |
| MC38 | Growth Inhibition Assay | 5 μM | 5 d | inhibits cell growth in a time-dependent manner | 19909744 | |
| U937 | Growth Inhibition Assay | 5-20 μM | 24-72 h | inhibits cell growth slightly | 18492113 | |
| HLE | Cytotoxity Assay | 0.001-20 μM | 48 h | induces cell cytotoxity in a dose-dependent manner | 18318443 | |
| HLF | Cytotoxity Assay | 0.001-20 μM | 48 h | induces cell cytotoxity in a dose-dependent manner | 18318443 | |
| Sf9 | Function assay | 1 hr | Inhibition of human His-tagged TGFbetaR1 T204D mutant expressed in Sf9 insect cells after 1 hr by HTRF assay, IC50 = 0.0037 μM. | 29422332 | ||
| Sf9 | Function assay | Inhibition of TGFbeta type receptor 1 ALK5 (T204D) expressed in Sf9 cells, IC50 = 0.069 μM. | 18314943 | |||
| Mv1Lu-p3TP-Lux | Antiproliferative assay | Antiproliferative activity against mink Mv1Lu-p3TP-Lux cells by luciferase reporter assay, IC50 = 0.18 μM. | 18314943 | |||
| NIH3T3 | Antiproliferative assay | Antiproliferative activity against mouse NIH3T3 cells by [3H]thymidine assay, IC50 = 0.21 μM. | 18314943 | |||
| Calu6 | Function assay | Inhibition of TGFbeta type receptor 1 in orally dosed human Calu6 cells xenografted mouse by IVTI pharmacokinetic assay, EC50 = 0.236 μM. | 18314943 | |||
| T-cells | Function assay | 1 hr | Inhibition of TGFbetaR1 in human primary T-cells assessed as TGFbeta-stimulated PSMAD phosphorylation preincubated for 1 hr followed by TGFbeta addition measured after 90 mins by Alpha screen assay, IC50 = 0.37 μM. | 29422332 | ||
| Mv1Lu | Function assay | 1 hr | Inhibition of TGFbetaR1 in mink Mv1Lu cells assessed as TGFbeta-stimulated PSMAD2 phosphorylation preincubated for 1 hr followed by TGFbeta addition measured after 15 mins, IC50 = 0.75 μM. | 29422332 | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 441.52 | Formel | C26H27N5O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 700874-71-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | C1CC2=C(C(=NN2C1)C3=CC=CC=N3)C4=C5C=CC(=CC5=NC=C4)OCCN6CCOCC6 | ||
Löslichkeit
|
In vitro |
DMSO
: 9 mg/mL
(20.38 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
TβRI
(Cell-free assay) 38 nM(Ki)
TβRII
(Cell-free assay) 300 nM(Ki)
|
|---|---|
| In vitro |
Die Behandlung mit LY2109761 führt zu einer dosisabhängigen Hemmung des geringen Verankerungswachstums von L3.6pl/GLT-Zellen, die bei 2 μM und 20 μM zu einer Hemmung von ~33% bzw. 73% führt, was bei einem Kombinationsindexwert von 0,36581 stark verstärkt werden kann. Die Blockade der TβRI/II-Kinaseaktivität mit dieser Verbindung unterdrückt sowohl die basale als auch die TGF-β1-stimulierte Migration und Invasion von L3.6pl/GLT-Zellen vollständig, verstärkt die ablösungsinduzierte Apoptosis nach 8 Stunden Behandlung um 26% und unterdrückt die TGF-β–induzierte Smad2-Phosphorylierung vollständig. Diese chemische Behandlung bei 1 nM ist ausreichend, um die Migration und Invasion, aber nicht die Adhäsion von hepatozellulären Karzinomzellen durch Erhöhung der E-Cadherin-Expression signifikant zu blockieren. Die Vorbehandlung verbessert die Radiosensitivität von Glioblastomzellen über die TGF-β-Signalblockade. Diese Verbindung reduziert die Selbsterneuerung und Proliferation von GBM-abgeleiteten Krebsstammzellen (CSLC), was bei Kombination mit Bestrahlung signifikant verstärkt werden kann. |
| In vivo |
Die Verabreichung von LY2109761 (50 mg/kg) allein oder in Kombination reduziert das Tumorvolumen um ~70% bzw. ~90%, verlängert das Überleben mit einer mittleren Überlebensdauer von 45,0 Tagen bzw. 77,5 Tagen und reduziert spontane abdominale Metastasen im L3.6pl/GLT-Xenograft-Mausmodell. In Übereinstimmung mit dem In-vitro-Effekt hemmt die Verabreichung dieser Verbindung allein oder in Kombination mit Bestrahlung das Tumorwachstum im orthotopischen CSLC-Glioblastommodell um 43,4% bzw. 76,3%, verringert die Tumorinvasion und die Mikrovaskulardichte des Tumors und verstärkt die strahleninduzierte Tumorwachstumsverzögerung im U87MG-Xenograft-Mausmodell signifikant. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | CDK2 / CDK4 / Cyclin D1 / p-Rb β-catenin / MMP-9 / MMP-2 / nm23 / uPA / COX-2 E-cadherin p-Smad2 / Smad |
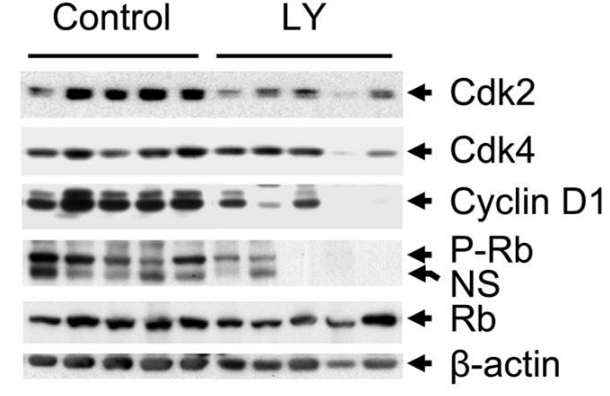
|
19909744 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
