nur für Forschungszwecke
Phenothiazine Dopamine Receptor Antagonist
Kat.-Nr.S4251
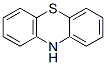
Chemische Struktur
Molekulargewicht: 199.27
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere Dopamine Receptor Inhibitoren | MPTP Hydrochloride Trifluoperazine Trifluoperazine 2HCl Penfluridol Sulpiride Levosulpiride SCH-23390 hydrochloride Domperidone Rotundine Azaperone |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 199.27 | Formel | C12H9NS |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 92-84-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | ENT 38 | Smiles | C1=CC=C2C(=C1)NC3=CC=CC=C3S2 | ||
Löslichkeit
|
In vitro |
DMSO
: 40 mg/mL
(200.73 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
D2 receptor
|
|---|---|
| In vitro |
Phenothiazine ersetzen meist an Position 10 mit den Dialkylaminoalkylgruppen und zusätzlich an Position 2 mit kleinen Gruppen und zeigen wertvolle Aktivitäten wie Neuroleptika, Antiemetika, Antihistaminika, Antipuritika, Analgetika und Antihelmintika. 2-Trifluoromethyl-10-(4-aminobutyl)phenothiazine hemmt S. cerevisiae-Stämme und T. mentagrophites mit einem MIC von 0,4 μg/mL bzw. 1,5 μg/mL. 10-Carbamoylalkylderivate zeigen signifikante Aktivitäten gegen Gram-positive Bacillus subtilis mit MICs im Bereich von 7,8 μg/mL–30 μg/mL. Die tetrazyklischen Verbindungen (modifiziert mit dem Naphthochinonring) zeigen eine signifikante antibakterielle Aktivität gegen S. aureus mit einem MIC50 von 12,5 μg/mL. Diese Verbindungen mit dem Butylen-Linker sind wirksamer als mit dem Propylen-Linker, wobei das 2-Chlor-10-chlorethylureidobutyl-Derivat eine GI50 von 1,4 μM und 1,6 μM gegen 4 Leukämiezelllinien und 7 Darmkrebszelllinien ergibt. 10-Amino(hydroxy)propylderivate (5 μM) induzieren nach 2-tägiger Inkubation eine ausgeprägte G2/M-Phase des Zellzyklusarrests, gefolgt vom Zelltod in menschlich transformierten WI38VA-Zellen. Diese Arzneimittelklasse wird im Körper vor der Ausscheidung umfassend metabolisiert, hauptsächlich durch Ringhydroxylierung, Ringsulphoxidation, N-Demethylierung, N-Oxidation, Sulfat- und Glucuronidkonjugation. Sie haben erheblich geringere Bindungsaffinitäten zu α2-Adrenozeptoren als zu dopamine D2 receptors und al-Adrenozeptoren. Diese Verbindungen zeigen eine signifikante In-vitro-Aktivität gegen anfällige, polydrug- und multiresistente Stämme von M. tuberculosis sowie eine Verstärkung der Aktivität einiger Mittel, die für die Erstlinienbehandlung eingesetzt werden.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
