nur für Forschungszwecke
Verteporfin YAP-Inhibitor
Kat.-Nr.S1786
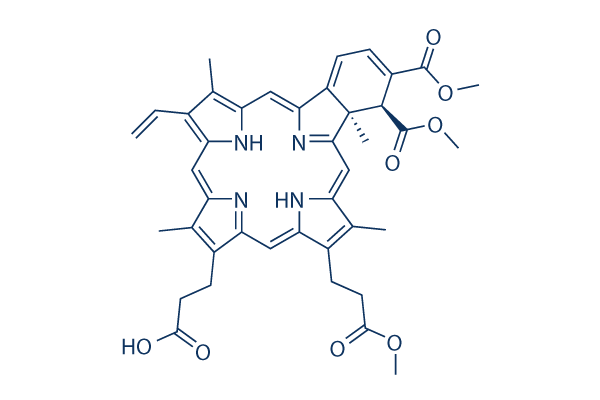
Chemische Struktur
Molekulargewicht: 718.79
Qualitätskontrolle
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HL-60 | Function assay | ~100 ng/mL | DMSO | increases DNA fragmentation levels | 10607710 | |
| HL-60 | cytotoxicity assay | ~100 ng/mL | DMSO | inhibits cell viability | 10607710 | |
| Jurkat | Apoptosis assay | ~280 nM | DMSO | induces a Bcl-2-dependent apoptosis | 11245415 | |
| RIF-1 | Function assay | 1 μg/ml | DMSO | decreases oxygen consumption | 12615718 | |
| RIF-1 | cytotoxicity assay | 1 μg/ml | DMSO | decrease to 20 ± 5% cell survival | 12615718 | |
| SVEC4-10 | Function assay | 200 ng/ml | DMSO | induces microtubule depolymerization | 16467106 | |
| SVEC4-10 | Function assay | 200 ng/ml | DMSO | induces stress actin fiber formation | 16467106 | |
| ARPE-19 | cytotoxicity assay | ~0.1 μg/ml | DMSO | shows a dose-dependent toxicity | 16987905 | |
| ARPE-19 | Function assay | 0.01 μg/ml | DMSO | increases VEGF and reduces PEDF expression | 16987905 | |
| Y-79 | Growth inhibitory assay | ~1 μg/ml | DMSO | decreases retinoblastoma cell proliferation | 18579764 | |
| WERI-Rb1 | Growth inhibitory assay | ~1 μg/ml | DMSO | decreases retinoblastoma cell proliferation | 18579764 | |
| RB247C3 | Growth inhibitory assay | ~1 μg/ml | DMSO | decreases retinoblastoma cell proliferation | 18579764 | |
| RB355 | Growth inhibitory assay | ~1 μg/ml | DMSO | decreases retinoblastoma cell proliferation | 18579764 | |
| RB383 | Growth inhibitory assay | ~1 μg/ml | DMSO | decreases retinoblastoma cell proliferation | 18579764 | |
| hFibro | cytotoxicity assay | 0.5 µg/ml | DMSO | decreases viability by 86,5% | 23441114 | |
| pTMC | cytotoxicity assay | 0.5 µg/ml | DMSO | decreases viability by 92.9% | 23441114 | |
| hTMC | cytotoxicity assay | 0.5 µg/ml | DMSO | decreases viability by 88.9% | 23441114 | |
| ARPE-19 | cytotoxicity assay | 0.5 µg/ml | DMSO | decreases viability by 55.5% | 23441114 | |
| Panc-1 | Growth inhibitory assay | 10 μM | DMSO | inhibits cell proliferation | 24069069 | |
| MIA PaCa-2 | Growth inhibitory assay | 10 μM | DMSO | inhibits cell proliferation | 24069069 | |
| BxPC-3 | Growth inhibitory assay | 10 μM | DMSO | inhibits cell proliferation completely | 24069069 | |
| SU86.86 | Growth inhibitory assay | 10 μM | DMSO | inhibits cell proliferation completely | 24069069 | |
| MCF-7 | Autophagy assay | 10 μM | DMSO | inhibits gemcitabine-induced autophagy | 24069069 | |
| WERI | Growth inhibitory assay | ~10 μg/ml | DMSO | inhibits growth of retinoblastoma cells | 24837142 | |
| WERI | Function assay | ~10 μg/ml | DMSO | blocks cell cycle progression | 24837142 | |
| Y-79 | Function assay | ~10 μg/ml | DMSO | blocks cell cycle progression | 24837142 | |
| Y-79 | Function assay | ~10 μg/ml | DMSO | affects YAP-TEAD proto-oncogene pathway | 24837142 | |
| Y-79 | Function assay | ~10 μg/ml | DMSO | down-regulates pluripotency marker OCT-4 | 24837142 | |
| Phototoxicity assay | B16F10 | 24 hrs | IC50 = 1.07 μM | 27136389 | ||
| Phototoxicity assay | B16F10 | 24 hrs | IC50 = 1.2 μM | 27136389 | ||
| Phototoxicity assay | A375 | 24 hrs | IC50 = 2.06 μM | 27136389 | ||
| Dark toxicity assay | B16F10 | 48 hrs | IC50 = 24.92 μM | 27136389 | ||
| Dark toxicity assay | B16F10 | 48 hrs | IC50 = 25.03 μM | 27136389 | ||
| Dark toxicity assay | A375 | 48 hrs | IC50 = 36.33 μM | 27136389 | ||
| qHTS assay | TC32 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for TC32 cells | 29435139 | |||
| qHTS assay | U-2 OS | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for U-2 OS cells | 29435139 | |||
| qHTS assay | A673 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for A673 cells | 29435139 | |||
| qHTS assay | DAOY | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for DAOY cells | 29435139 | |||
| qHTS assay | Saos-2 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Saos-2 cells | 29435139 | |||
| qHTS assay | BT-37 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-37 cells | 29435139 | |||
| qHTS assay | RD | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for RD cells | 29435139 | |||
| qHTS assay | SK-N-SH | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-SH cells | 29435139 | |||
| qHTS assay | BT-12 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for BT-12 cells | 29435139 | |||
| qHTS assay | MG 63 (6-TG R) | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for MG 63 (6-TG R) cells | 29435139 | |||
| qHTS assay | OHS-50 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for OHS-50 cells | 29435139 | |||
| qHTS assay | Rh41 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for Rh41 cells | 29435139 | |||
| qHTS assay | SJ-GBM2 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SJ-GBM2 cells | 29435139 | |||
| qHTS assay | SK-N-MC | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for SK-N-MC cells | 29435139 | |||
| qHTS assay | LAN-5 | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for LAN-5 cells | 29435139 | |||
| Antitumor assay | B16F10 | 2 mg/kg | 2 hrs | Antitumor activity against B16F10 cells implanted in C57BL/6 mouse assessed as tumor growth inhibition at 2 mg/kg, iv administered for 2 hrs followed by irradiation with laser at 150 J/cm'2 for 10 mins | 27136389 | |
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 718.79 | Formel | C41H42N4O8 |
Lagerung (Ab dem Eingangsdatum) | 3 years-20°C (in the dark)powder |
|---|---|---|---|---|---|
| CAS-Nr. | 129497-78-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | CL 318952 | Smiles | COC(=O)CCC1=C(C)C2=CC3=NC(=CC4=C(C)C(=C([NH]4)C=C5N=C(C=C1[NH]2)C(=C5C)CCC(O)=O)C=C)C6=CC=C(C(C(=O)OC)C36C)C(=O)OC | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(139.12 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
VDA
(Endothelial cells) YAP/TEAD interaction
|
|---|---|
| In vitro |
Verteporfin ist etwa viermal effizienter bei der Absorption von Licht bei Wellenlängen, die Gewebe am besten durchdringen (d.h. um 700 nm), und bietet somit eine viel höhere zytotoxische Wirkung als Hämatoporphyrin (10-mal mehr in menschlichen adhärenzabhängigen Zelllinien). Diese Verbindung ist lipophil und wird im Vergleich zu normalen oder ruhenden Zellen leichter von malignen oder aktivierten Zellen aufgenommen. Es bindet mit LDL zu einem Komplex, der dann von proliferierenden Zellen (z.B. neovaskulären Endothelzellen) wahrscheinlich über LDL-Rezeptoren und Endozytose aufgenommen wird. Diese Therapie erreicht eine vollständige angiographische Okklusion des neovaskulären Kompartiments durch Thrombose von Gefäßkanälen nach selektiver endothelialer Schädigung. Es induziert selektiv reproduzierbare und isolierte Choriokapillarokklusion ohne Veränderung der darüber liegenden Photorezeptoren oder Ganglienzellen, wie Licht- und Elektronenmikroskopie zeigen. Diese Chemikalie, kombiniert mit Licht, zeigt schnell Apoptosis related Veränderungen, die sich in der Aktivierung von Caspase-3 und Caspase-9 sowie der PARP-Spaltung in HL-60-Zellen widerspiegeln, Veränderungen, die durch den allgemeinen Caspase-Inhibitor ZVAD.fmk blockiert werden. |
| In vivo |
Verteporfin kann zur angiographischen Visualisierung von choroidalen Gefäßen und CNV verwendet werden, was zeigt, dass der Photosensitizer sich schnell in experimenteller CNV bei Affen anreichert. Diese Verbindung reichert sich schnell in der etablierten Vaskulatur der Choroidea, des RPE und der Photorezeptoren von Kaninchenaugen an. Sie erreicht maximale Gewebespiegel innerhalb von 3 Stunden nach intravenöser Injektion, gefolgt von einem schnellen Rückgang innerhalb von 24 Stunden bei Mäusen. Diese Chemikalie wird in vivo zu einer weniger aktiven Form metabolisiert und sehr schnell ausgeschieden, hauptsächlich im Kot und ein sehr kleiner Teil im Urin. Die Therapie verhindert effektiv und selektiv das Auslaufen von Fluoreszein-Farbstoff aus experimentell induzierter CNV bei Affen. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | ECAD / Vimentin / Sox2 / CD44 / CD133 c-Myc / Bcl-2 p-S6(S240/244) / p-4EBP1(S65) beta-catenin |
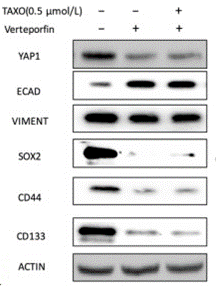
|
30467925 |
| Growth inhibition assay | Cell viability |
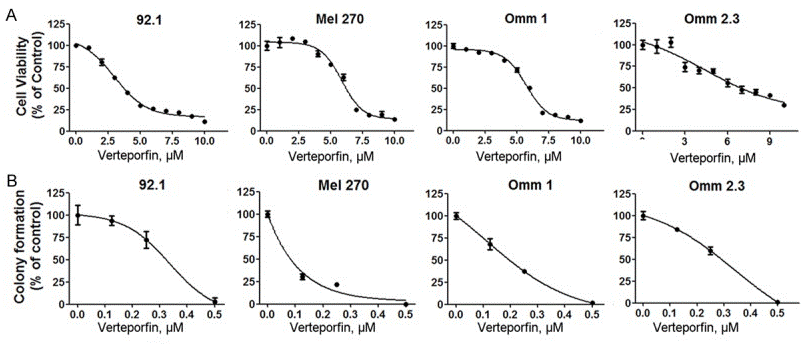
|
28042502 |
| Immunofluorescence | p-YAP(Y357) Calreticulin YAP1 |
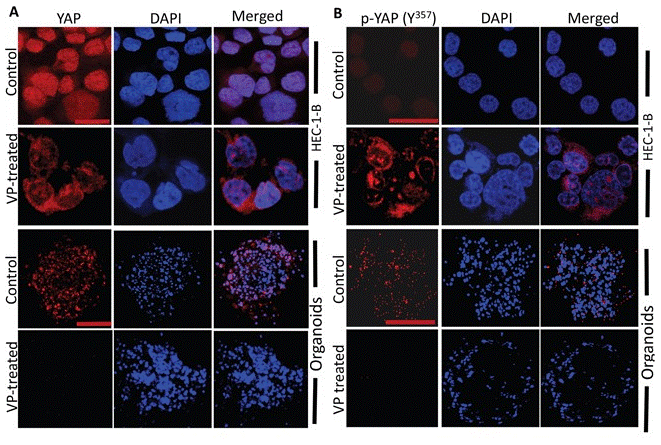
|
28404908 |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04590664 | Recruiting | Glioblastoma|Recurrent Glioblastoma |
Emory University|National Cancer Institute (NCI) |
January 15 2021 | Phase 1|Phase 2 |
| NCT03797547 | Unknown status | Myopic Choroidal Neovascularisation |
Poitiers University Hospital |
June 22 2018 | -- |
| NCT01846273 | Completed | Age-related Macular Degeneration|Polypoidal Choroidal Vasculopathy |
Novartis Pharmaceuticals|Novartis |
August 7 2013 | Phase 4 |
| NCT00423189 | Terminated | Age-Related Macular Degeneration |
David M. Brown M.D.|Novartis Pharmaceuticals|Greater Houston Retina Research |
January 2007 | Phase 4 |
| NCT00403442 | Terminated | Macular Degeneration |
Vitreous -Retina- Macula Consultants of New York|QLT Inc. |
September 2006 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
