nur für Forschungszwecke
10058-F4 c-Myc Inhibitor
Kat.-Nr.S7153
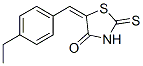
Chemische Struktur
Molekulargewicht: 249.35
Qualitätskontrolle
| Verwandte Ziele | CDK HSP PD-1/PD-L1 ROCK Wee1 DNA/RNA Synthesis Microtubule Associated Ras KRas Aurora Kinase |
|---|---|
| Weitere Myc Inhibitoren | MYCi975 10074-G5 MYCi361 EN4 Mycro 3 APTO-253 ML327 MYCMI-6 BTYNB Cpd. 37 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| REH | Function assay | 0-400 µM | 48 h | reduced the metabolic activity, IC50=400 μM | 30957273 | |
| Nalm-6 | Function assay | 0-400 µM | 48 h | reduced the metabolic activity, IC50=430 μM | 30957273 | |
| Jurkat | Function assay | 60 μM | 24 h | c-Myc expression levels treated with VPA (0, 0.8 and 1.6 mM) combined with 60 μM 10058-F4 decreased further compared with the corresponding controls | 25120723 | |
| CCRF-CEM | Function assay | 60 μM | 24 h | c-Myc expression levels treated with VPA (0, 0.8 and 1.6 mM) combined with 60 μM 10058-F4 decreased further compared with the corresponding controls | 25120723 | |
| HL-60 | Function assay | 60 and 100 μM | 24 hours | decreased levels of c-Myc proteins | 17046567 | |
| U937 | Function assay | 60 and 100 μM | 24 hours | decreased levels of c-Myc proteins | 17046567 | |
| NB4 | Function assay | 60 and 100 μM | 24 hours | decreased levels of c-Myc proteins | 17046567 | |
| NB1643 | qHTS assay | qHTS of pediatric cancer cell lines to identify multiple opportunities for drug repurposing: Primary screen for NB1643 cells | 29435139 | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 249.35 | Formel | C12H11NOS2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 403811-55-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CCC1=CC=C(C=C1)C=C2C(=O)NC(=S)S2 | ||
Löslichkeit
|
In vitro |
DMSO
: 50 mg/mL
(200.52 mM)
Ethanol : 1 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
c-Myc
(Cell-free assay) |
|---|---|
| In vitro |
10058-F4 hemmt das Wachstum von Leukämiezellen und die Dimerisierung von Myc und Max. Diese Verbindung induziert den Cell Cycle-Arrest und die Apoptose von AML-Zellen. Sie arretiert AML-Zellen in der G0/G1-Phase, reguliert die c-Myc-Expression herunter und die CDK-Inhibitoren p21 und p27 hoch. Gleichzeitig induziert diese Chemikalie Apoptose durch Aktivierung des mitochondrialen Signalwegs, was sich durch eine Herunterregulierung von Bcl-2, eine Hochregulierung von Bax, die Freisetzung von zytoplasmatischem Cytochrom C und die Spaltung von Caspase 3, 7 und 9 zeigt. Darüber hinaus induziert sie auch die myeloische Differenzierung, möglicherweise durch die Aktivierung mehrerer Transkriptionsfaktoren. Ähnlich konnte die durch diese Verbindung induzierte Apoptose und Differenzierung auch in primären AML-Zellen beobachtet werden. Sie senkt die c-Myc-Proteinspiegel, hemmt die Proliferation von HepG2-Zellen wahrscheinlich durch Hochregulierung des Cyclin-abhängigen Kinase (cdk)-Inhibitors p21WAF1 und senkt die intrazellulären Spiegel von [alpha]-Fetoprotein (AFP). Die Behandlung mit dieser Chemikalie reguliert auch die humane Telomerase-Reverse-Transkriptase (hTERT) auf transkriptioneller Ebene herunter. Zusätzlich zur Hemmung der Proliferation von HepG2-Zellen erhöht sie die Empfindlichkeit gegenüber konventionellen chemotherapeutischen Mitteln. |
| In vivo |
Maximale Plasmakonzentrationen von 10058-F4 von ungefähr 300 μM werden 5 Minuten nach einer einzelnen i.v.-Dosis beobachtet und sanken innerhalb von 360 Minuten unter die Nachweisgrenze. Die Plasma-Konzentrations-Zeit-Daten lassen sich am besten durch ein Zwei-Kompartiment-Modell, offen und linear, annähern. Die höchsten Gewebekonzentrationen dieser Verbindung wurden in Fett, Lunge, Leber und Niere gefunden. Die maximalen Tumorkonzentrationen dieser Chemikalie waren mindestens zehnmal niedriger als die maximalen Plasmakonzentrationen. Acht Metaboliten dieser Verbindung wurden in Plasma, Leber und Niere identifiziert. Die terminale Halbwertszeit dieser Chemikalie beträgt ungefähr 1 Stunde, und das Verteilungsvolumen ist >200 ml/kg. Nach i.v.-Behandlung von Mäusen mit 20 oder 30 mg/kg dieser Verbindung wurde keine signifikante Hemmung des Tumorwachstums beobachtet. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | PARP / Caspase-3 / Myc Cyclin D2 / Cyclin D3 / p-21 / c-Myc / p-AKT / AKT p-EGFR / HIF-1α / c-Myc / Glut-1 |
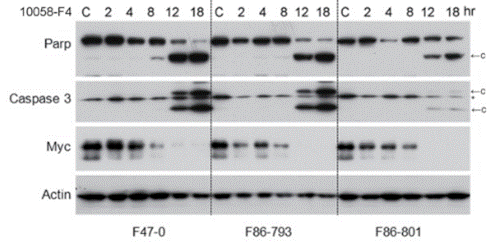
|
25793663 |
| Growth inhibition assay | Cell viability |
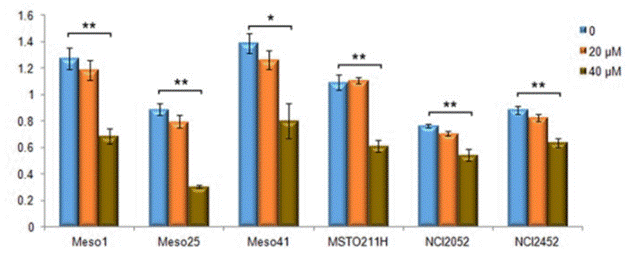
|
28861328 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
