nur für Forschungszwecke
Amonafide Topoisomerase Inhibitor
Kat.-Nr.S1367
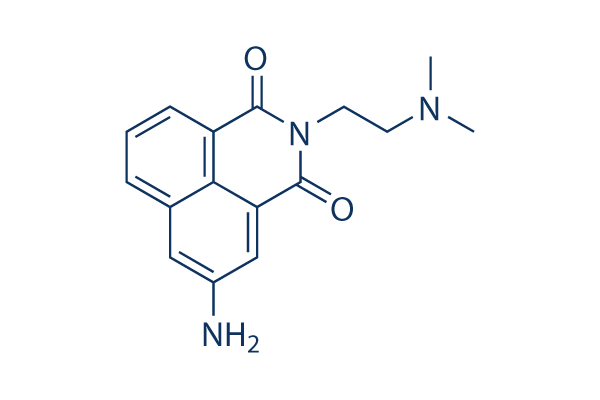
Chemische Struktur
Molekulargewicht: 283.33
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere Topoisomerase Inhibitoren | Camptothecin (CPT) Betulinic acid Beta-Lapachone (S)-10-Hydroxycamptothecin Voreloxin (SNS-595) hydrochloride Ellagic acid Cu(II)-Elesclomol Hydroxy Camptothecine Rubitecan Belotecan (CKD-602) hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 283.33 | Formel | C16H17N3O2 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 69408-81-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | NSC308847,AS1413 | Smiles | CN(C)CCN1C(=O)C2=CC=CC3=CC(=CC(=C32)C1=O)N | ||
Löslichkeit
|
In vitro |
DMSO
: 57 mg/mL
(201.17 mM)
Ethanol : 4 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Topo II
|
|---|---|
| In vitro |
Durch eine Topoisomerase II-vermittelte Reaktion führt die Amonafide-Behandlung zu DNA-Einzelstrangbrüchen (SSB), Doppelstrangbrüchen (DSB) und DNA-Protein-Vernetzungen in menschlichen myeloischen Leukämiezellen. Diese Compound-Behandlung hemmt die Koloniebildung der Leukämiezelllinien und des normalen menschlichen Knochenmark-GM-CFC dosisabhängig. Es führt selbst bei 100 μM nicht zu einer Topoisomerase I-vermittelten DNA-Spaltung. Die m-AMSA-resistente Linie ist weniger als 2-fach resistent gegen diese Verbindung Diese Chemikalie stört die DNA-Bruch-Wiedervereinigungsaktivität der Säugetier-DNA-Topoisomerase II, was zu einer Stimulation der DNA-Spaltung führt. Im Vergleich zu denen anderer Antitumor-Medikamente sind die durch diese Verbindung stimulierten Spaltungsintensitätsmuster deutlich unterschiedlich. Es bevorzugt stark ein Cytosin und schließt stattdessen Guanine und Thymine an Position -1 aus, mit einer geringeren Präferenz für ein Adenin an Position +1. Die durch dieses Mittel induzierte Topoisomerase II-vermittelte DNA-Spaltung wird durch 1 mM ATP nur geringfügig (weniger als 3-fach) beeinflusst, was darauf hindeutet, dass es sich im Gegensatz zu Doxorubicin, Etoposid und Mitoxantron um einen ATP-unempfindlichen Topoisomerase II-Inhibitor handelt. Diese Verbindung hemmt signifikant das Wachstum von HT-29-, HeLa- und PC3-Zellen mit IC50-Werten von 4,67 μM, 2,73 μM bzw. 6,38 μM. Es wird im Gegensatz zu den klassischen Topoisomerase II-Inhibitoren (Daunorubicin, Doxorubicin, Idarubicin, Etoposid und Mitoxantron) nicht durch P-Glykoprotein-vermittelten Efflux beeinflusst.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01066494 | Unknown status | Acute Myeloid Leukemia |
Antisoma Research |
January 2010 | Phase 2 |
| NCT00273884 | Completed | Acute Myeloid Leukemia |
Xanthus Pharmaceuticals Inc. |
August 2005 | Phase 2 |
| NCT00087854 | Completed | Prostate Cancer |
Xanthus Pharmaceuticals Inc. |
March 2004 | Phase 1|Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
