nur für Forschungszwecke
Betulinic acid Topoisomerase Inhibitor
Kat.-Nr.S3603
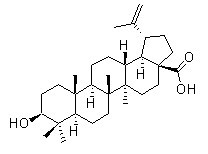
Chemische Struktur
Molekulargewicht: 456.7
Qualitätskontrolle
| Verwandte Ziele | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere Topoisomerase Inhibitoren | Camptothecin (CPT) Beta-Lapachone (S)-10-Hydroxycamptothecin Amonafide Voreloxin (SNS-595) hydrochloride Ellagic acid Cu(II)-Elesclomol Hydroxy Camptothecine Rubitecan Belotecan (CKD-602) hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 456.7 | Formel | C30H48O3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 472-15-1 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
Löslichkeit
|
In vitro |
DMSO
: 20 mg/mL
(43.79 mM)
Ethanol : 10 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
HIV-1
1.4 μM(EC50)
Eukaryotic topoisomerase I
5 μM
Aminopeptidase N
7.3 μM
|
|---|---|
| In vitro |
Betulinic acid zeigt Anti-HIV-Aktivität, indem es die HIV-Replikation in H9-Lymphozyten mit einem EC50-Wert von 1,4 μM blockiert und das Wachstum uninfizierter H9-Zellen mit einem IC50-Wert von 13 μM hemmt. Diese Verbindung wirkt auch als Anti-Melanom-Mittel, indem sie die Aminopeptidase-N-Aktivität mit einer IC50 von 7,3 μM hemmt. Darüber hinaus hemmt es die Aktivität der eukaryotischen Topoisomerase I mit einer IC50 von 5 μM und kann als starker Kandidat für ein Antitumormittel eingesetzt werden.
|
| Kinase-Assay |
Topoisomerase I-DNA-Interaktion
|
|
Ein geglühter 25-Mer-Duplex aus Oligonukleotid-1 und Oligonukleotid-2 wird 15 Minuten lang bei 8 °C mit 25 oder 50 Einheiten Rattenleber-Topoisomerase I in Anwesenheit oder Abwesenheit von Betulinic acid in Bindungspuffer inkubiert. Nach der Inkubation werden die Reaktionsgemische in einem 7%igen nicht-denaturierenden Polyacrylamidgel bei 4 °C in 0,167 × TBE-Puffer elektrophoretisch getrennt und die DNA-Banden mit Ethidiumbromid gefärbt
|
|
| In vivo |
Betulinic acid hemmt das Wachstum von Prostatakrebszellen und Tumoren (Xenotransplantate) bei athymischen Nacktmäusen mit LNCaP-Zellen, und dies ist teilweise auf die Proteasom-abhängige Herunterregulierung von Sp1, Sp3, Sp4 und mehreren Sp-regulierten Genen zurückzuführen.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
