nur für Forschungszwecke
Atropine sulfate monohydrate ADC Cytotoxin Inhibitor
Kat.-Nr.S2130
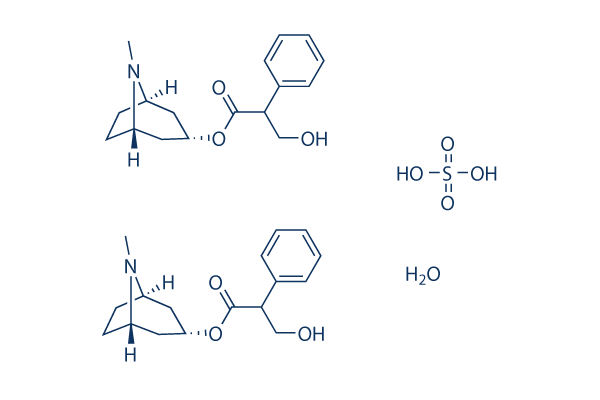
Chemische Struktur
Molekulargewicht: 694.83
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) |
|---|---|
| Weitere ADC Cytotoxin Inhibitoren | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 694.83 | Formel | 2(C17H23NO3).H2O.H2SO4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 5908-99-6 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN1C2CCC1CC(C2)OC(=O)C(CO)C3=CC=CC=C3.CN1C2CCC1CC(C2)OC(=O)C(CO)C3=CC=CC=C3.O.OS(=O)(=O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 139 mg/mL
(200.04 mM)
Water : 139 mg/mL Ethanol : 139 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
mAChR
2.5 nM
|
|---|---|
| In vitro |
Atropine erhöht die Freisetzung des Neurotransmitters Dopamin in vitro bei 100–500 mM in den Superfusat und in vivo bei 250 mg in den Glaskörper. Atropine induziert in der In-vitro-Präparation eine Spreading-Depression (SD). Atropine reduziert die ERG b- und d-Welle, führt zu gedämpften Oszillationen der RPE-Potenziale und kehrt die ERG c-Welle um. Atropine unterdrückt Myopie nur bei Dosen, bei denen schwere unspezifische Nebenwirkungen in der Netzhaut beobachtet werden.
|
| In vivo |
Atropine (1,0 mg/kg, i.p.), aber nicht Methylatropine (1,0 mg/kg, i.p.), verhindert die Retention-Erhöhung, die durch beide Dosen des Anticholinesterase induziert wird, wenn es Mäusen unmittelbar nach dem Training verabreicht wird. Atropine-Verabreichung verhindert effektiv Bradykardie und einen Herzblock zweiten Grades, induziert aber Pulsus alternans und Hypertonie bei Hunden. Atropine hat in Gegenwart von 10 nM Neostigmin keine Wirkung auf die durch Handling induzierte Acetylcholinausscheidung, führt aber in Gegenwart von 100 nM und 1000 nM Neostigmin bei Ratten zu stärkeren und längeren Erhöhungen. Atropine blockiert nicht nur die durch CGS induzierten Zunahmen des REM-Schlafs (rapid eye movement), sondern neigt auch dazu, den REM-Schlaf im Vergleich zu Atropine vor Salzlösung bei Ratten zu verringern. Atropine verringert die Erschöpfungszeit bei intakten Ratten um 67 % und bei adrenodemedullierten (ADM) Ratten um 96,2 % und reduziert auch die trainingsinduzierte Freisetzung von Hypophysenprolaktin (PRL) sowohl bei intakten (50 %) als auch bei ADM-Ratten (90 %).
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT06291363 | Not yet recruiting | Opioid Use Unspecified|Anesthesia|Nociceptive Pain |
Ciusss de L''Est de l''Île de Montréal |
April 4 2024 | Phase 4 |
| NCT06263946 | Recruiting | Myopia |
Essilor International |
March 22 2024 | Not Applicable |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
