nur für Forschungszwecke
Luteolin ADC Cytotoxin Inhibitor
Kat.-Nr.S2320
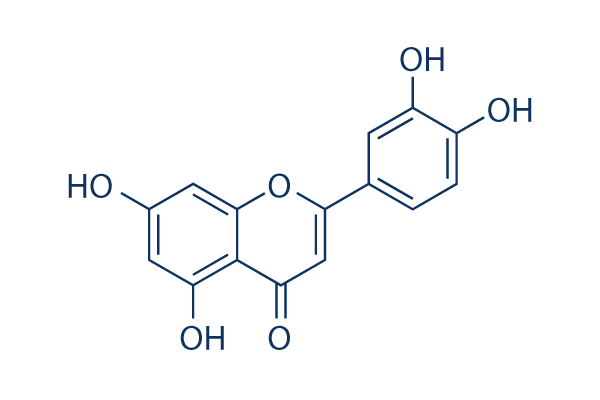
Chemische Struktur
Molekulargewicht: 286.24
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere ADC Cytotoxin Inhibitoren | Triptolide SN-38 (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside Sacituzumab-govitecan |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| mouse RAW264.7 cells | Function assay | 2 h | Inhibition of NO production in LPS-stimulated mouse RAW264.7 cells pre-incubated for 2 hrs before LPS stimulation for 24 hrs by Griess assay method, IC50=0.21 μM | |||
| HEK293 FS cells | Function assay | Inhibition of NOX4 expressed in HEK293 FS cells assessed as H2O2 production by H2O2/Tyr/LPO assay, IC50=0.85 μM | ||||
| CHO cells | Function assay | Agonist activity at rat DAT expressed in CHO cells, EC50=1.45 μM | ||||
| human MV4-11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human MV4-11 cells harboring FLT3 mutation after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=1.76 μM | |||
| HEK293 cells | Function assay | 24 h | Agonist activity at mouse PPARgamma expressed in HEK293 cells co-expressing with Gal4 reporter vector after 24 hrs by dual-luciferase reporter assay, EC50=2.3 μM | |||
| human U2OS cells | Function assay | 5 h | Agonist activity at GPR35 receptor in human U2OS cells coexpressing Gal4-VP16-TEV assessed as beta arrestin translocation after 5 hrs by beta lactamase reporter gene assay, EC50=3.2 μM | |||
| RBL-2H3 cells | Function assay | Inhibitory activity against IL-4 production in RBL-2H3 cells was determined, IC50=3.7 μM | ||||
| human mast cells | Function assay | Inhibition of SYK in human mast cells assessed as reduction in mast cell degranulation, EC50=4.5 μM | ||||
| human LNCAP cells | Function assay | Downregulation of prostate specific antigen secretion in human LNCAP cells, IC50=5 μM | ||||
| rat H9c2 cells | Function assay | 24 h | Cytoprotective activity against doxorubicin-induced cytotoxicity in rat H9c2 cells assessed as cell viability after 24 hrs by MTT assay, EC50=5.53 μM | |||
| human HT-29 cells | Function assay | 10 mins | Agonist activity at GPR35 receptor in human HT-29 cells after 10 mins by dynamic mass redistribution assay, EC50=7.24 μM | |||
| human RS4:11 cells | Cytotoxicity assay | 72 h | Cytotoxicity against human RS4:11 cells harboring wild type FLT3 after 72 hrs by tetrazolium based Ez CyTox cell viability assay, GI50=7.25 μM | |||
| NCI-H460 cells | Function assay | 2-20 h | Inhibition of ABCG2 expressed in human NCI-H460 cells assessed as inhibition of PhA accumulation after 2 to 20 hrs relative to fumitremorgin C, IC50=8.9 μM | |||
| human H9 cells | Function assay | 3 days | Antiviral activity against HIV1 3B infected in human H9 cells assessed as inhibition of viral replication after 3 days by p24 antigen capture assay, EC50=10 μM | |||
| MDCK cells | Cytotoxicity assay | Cytotoxicity against MDCK cells by MTT assay, CC50=12.44 μM | ||||
| mouse B16-4A5 cells | Function assay | 72 h | Inhibition of theophylline-stimulated melanogenesis in mouse B16-4A5 cells after 72 hrs, IC50=14 μM | |||
| K562 cells | Growth inhibition assay | 5 days | Growth inhibition of K562 cells by XTT assay after 5 days, IC50=14.65 μM | |||
| human H9 cells | Cytotoxicity assay | 3 days | Cytotoxicity against human H9 cells after 3 days, IC50=16 μM | |||
| human HT-29 cells | Function assay | 10 mins | Desensitization of GPR35 receptor in human HT-29 cells assessed as inhibition of zaprinast-induced dynamic mass redistribution after 10 mins, IC50=18.6 μM | |||
| human U937 cells | Proliferation assay | 72 h | Antiproliferative activity against human U937 cells after 72 hrs by WST-8 assay, IC50=20 μM | |||
| mouse HT22 cells | Function assay | 3 h | Neuroprotective activity in mouse HT22 cells assessed as t-BOOH-induced toxicity at 40 uM preincubated for 3 hrs followed by t-BOOH induction measured after 9 hrs by MTT assay | |||
| human THP1 cells | Function assay | 20 μM | 1 h | Downregulation of TPA-induced NOX2 mRNA expression in human THP1 cells at 20 uM incubated for 1 hr prior to TPA challenge measured after 24 hrs by RT-PCR analysis | ||
| MDA-MB-231 cells | Function assay | 5 μM | 16 h | Inhibition of PMA-stimulated NF-kappaB signaling (unknown origin) expressed in MDA-MB-231 cells at 5 uM incubated for 16 hrs by luciferase reporter gene assay | ||
| HL60 cells | Proliferation assay | 30 μM | 48 h | Antiproliferative activity against human HL60 cells at 30 uM after 48 hrs by MTS assay | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 286.24 | Formel | C15H10O6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 491-70-3 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
Löslichkeit
|
In vitro |
DMSO
: 33 mg/mL
(115.28 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
PDE2
(Cell-free assay) 6.4 μM(Ki)
PDE5
(Cell-free assay) 9.5 μM(Ki)
PDE4
(Cell-free assay) 11.1 μM(Ki)
PDE3
(Cell-free assay) 13.9 μM(Ki)
PDE1
(Cell-free assay) 15.0 μM(Ki)
|
|---|---|
| In vitro |
Luteolin ist ein Flavonoid, das in Terminalia chebula gefunden wird und ein nicht-selektiver Phosphodiesterase PDE-Inhibitor für PDE1-5 mit einem Ki von 15,0 μM, 6,4 μM, 13,9 μM, 11,1 μM und 9,5 μM ist. Diese Verbindung hemmt die LPS-stimulierte TNF-alpha-Produktion mit einer IC50 von weniger als 1 μM. Sie hemmt die LPS-induzierte Phosphorylierung von Akt sowie IkappaBalpha. |
| In vivo |
LD50: Mäuse >2500mg/kg (i.g.) |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | FADD / PARP / Cleaved PARP Caspase-3 / Cleaved Caspase-3 / Caspase-8 / Cleaved Caspase-8 ERK / p-ERK / JNK / p-JNK / p38 / p-p38 / Bax / Bcl-2 p-VEGFR2 / p-mTOR / pS6K1 / p70S6K1 / pAKT / AKT / MMP-2 / MMP-9 p21 / Survivin / Cyclin D1 DNMT1 / DMNT3A / DNMT3B TET1 / TET2 / TET3 |
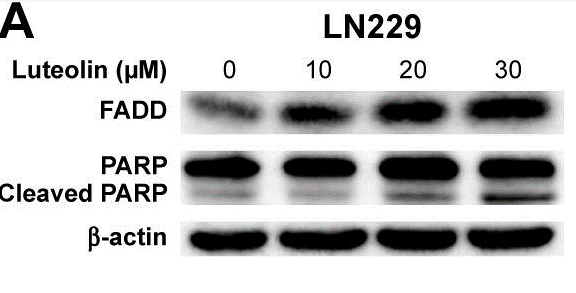
|
30992674 |
| Immunofluorescence | 5-hmC |
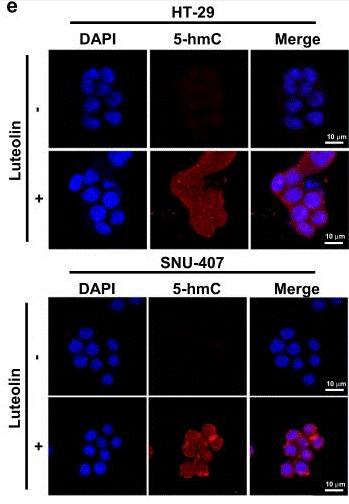
|
30988303 |
| Growth inhibition assay | Cell viability |
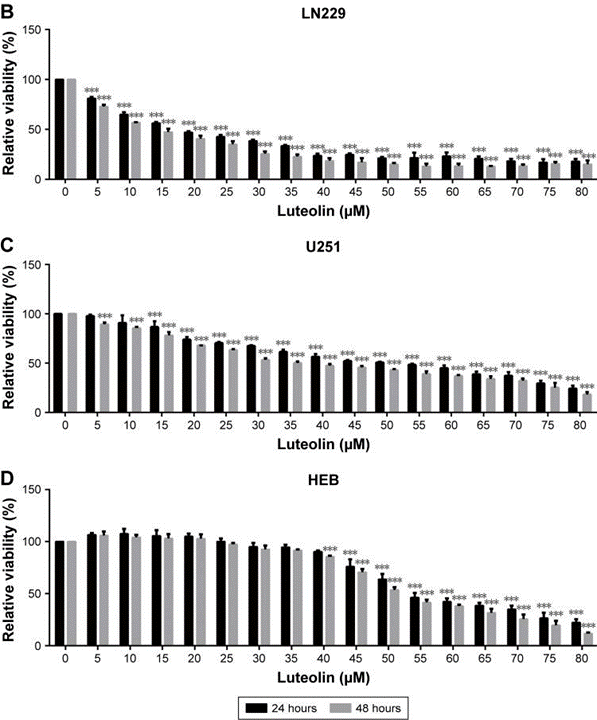
|
30992674 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
Häufig gestellte Fragen
Frage 1:
Would you please suggest a suitable vehicle to dissolve it for in vivo i.p. use?
Antwort:
Formula: 5% DMSO+40% PEG 300+5% Tween80+ddH2O, working Solution concentration: up to 7.5mg/ml, stable for 30min.
