nur für Forschungszwecke
Galanthamine HBr ADC Cytotoxin Inhibitor
Kat.-Nr.S1339
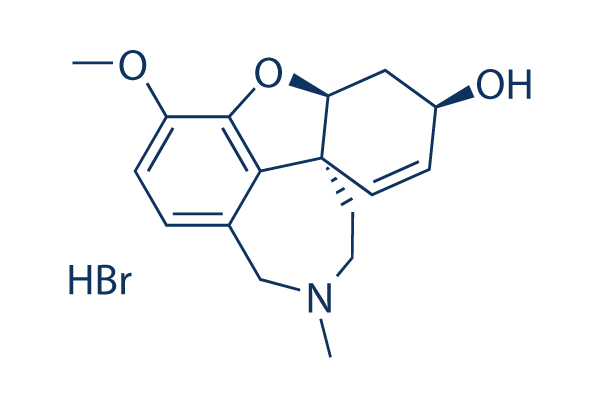
Chemische Struktur
Molekulargewicht: 368.27
Qualitätskontrolle
| Verwandte Ziele | Adrenergic Receptor AChR 5-HT Receptor COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) |
|---|---|
| Weitere ADC Cytotoxin Inhibitoren | Triptolide SN-38 Luteolin (+)-Bicuculline Rutin Artemisinin BHQ Pinocembrin Harmine hydrochloride Luteoloside |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 368.27 | Formel | C17H21NO3.HBr |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 1953-04-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CN1CCC23C=CC(CC2OC4=C(C=CC(=C34)C1)OC)O.Br | ||
Löslichkeit
|
In vitro |
Water : 10 mg/mL
DMSO
: Insoluble
Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
AChE
0.35 μM
|
|---|---|
| In vitro |
Galanthamin hat in der postmortalen menschlichen Gehirn-Frontalrinde und der Hippocampusregion einen IC50-Wert von 14 nM und 15 nM auf AChE gezeigt. Die Cholinesterase-Aktivität der roten Blutkörperchen in Blutproben von Neurochirurgie-Patienten wird durch Galanthamin in Gehirngewebeproben 10-mal stärker gehemmt. Galanthamin (1 μM) aktiviert Einzelkanäle mit Leitfähigkeiten von 18 und 30 pS in Outside-Out-Patches, die aus Dexamethason-Mausfibroblasten (M10-Zellen) herausgeschnitten wurden. Galanthamin wirkt als nicht-kompetitive nikotinische Rezeptoragonisten auf klonale Ratten-Phäochromozytom-Zellen (PC12). Galanthamin (50 μM) aktiviert Einzelkanalströme in Outside-Out-Patches, die aus klonalen PC12-Zellen herausgeschnitten wurden.
|
| In vivo |
Galantamin erhöht die Anzahl lebender Pyramidenneuronen nach Ischämie-Reperfusionsschaden signifikant. Galantamin reduziert TUNEL, aktive Caspase-3 und SOD-2 Immunreaktivität signifikant. Der nikotinische Antagonist Mecamylamin blockiert die schützenden Effekte von Galantamin. Die neuroprotektiven Effekte von Galantamin bleiben erhalten, selbst wenn es erst 3 Stunden nach der Ischämie verabreicht wird.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
