nur für Forschungszwecke
Aliskiren RAAS Inhibitor
Kat.-Nr.S5767
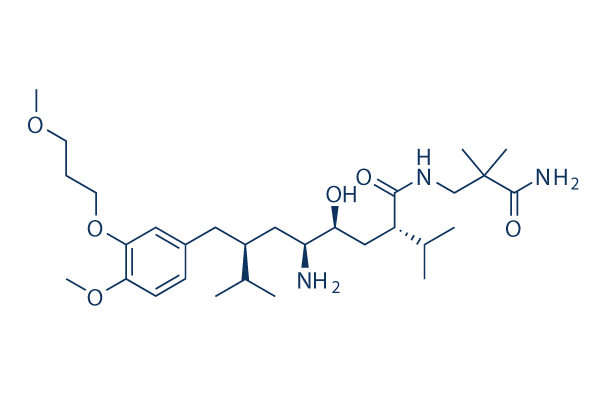
Chemische Struktur
Molekulargewicht: 551.76
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere RAAS Inhibitoren | Temocapril HCl Imidapril HCl VTP-27999 TFA Temocapril Zofenopril calcium Delapril Hydrochloride |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 551.76 | Formel | C30H53N3O6 |
Lagerung (Ab dem Eingangsdatum) | 3 years -20°C powder |
|---|---|---|---|---|---|
| CAS-Nr. | 173334-57-1 | -- | Lagerung von Stammlösungen |
|
|
| Synonyme | CGP 60536 | Smiles | CC(C)C(CC1=CC(=C(C=C1)OC)OCCCOC)CC(C(CC(C(C)C)C(=O)NCC(C)(C)C(=O)N)O)N | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(181.23 mM)
Ethanol : 100 mg/mL Water : 6 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
Renin
|
|---|---|
| In vitro |
Aliskiren ist die vierte Klasse von pharmakologischen Wirkstoffen, die die Funktion des RAAS modifizieren. Es ist ein Octanamid, der erste bekannte Vertreter einer neuen Klasse von vollständig nicht-peptidischen, niedermolekularen, oral aktiven Übergangszustands-Renin-Inhibitoren. Diese Verbindung besitzt eine gute Wasserlöslichkeit und geringe Lipophilie und ist resistent gegen den biologischen Abbau durch Peptidasen im Darm, Blutkreislauf und der Leber. Es hat eine 10.000-fach höhere Affinität für Renin als für andere Aspartat-Peptidasen. |
| In vivo |
In Kurzzeitstudien ist Aliskiren wirksam bei der Senkung des Blutdrucks, entweder allein oder in Kombination mit Valsartan und Hydrochlorothiazid, und hatte eine geringe Inzidenz schwerwiegender Nebenwirkungen. Diese Verbindung hat eine Halbwertszeit von ungefähr 40 Stunden, wodurch sie für eine einmal tägliche Dosierung geeignet ist, mit weniger Potenzial für einen Wirkungsverlust zwischen den Dosen als kürzer wirkende Mittel. Es zeigt eine orale Bioverfügbarkeit aufgrund seines niedrigen Molekulargewichts (609,8 Da) und seiner nicht-peptidischen Struktur, wodurch es widerstandsfähiger gegen den Abbau durch gastrointestinale Enzyme ist. Es wird jedoch immer noch schlecht resorbiert (orale Bioverfügbarkeit, ∼2,5 %). Diese Chemikalie ist zu 50 % proteingebunden, und das scheinbare Verteilungsvolumen beträgt 135 L. Es wird beim Menschen leicht (etwa 20 %) und bei Nagetieren zu etwa 50 % metabolisiert. Dieser Wirkstoff reduziert effektiv die funktionelle Plasma-Renin-Aktivität, indem er mit hoher Affinität an Renin bindet und es daran hindert, Angiotensinogen in Angiotensin I umzuwandeln. Die Hemmung von Renin durch diese Verbindung ist mit einer Reduktion der zirkulierenden Angiotensin I- und II-Spiegel verbunden, mit einem resultierenden Anstieg der Plasma-Renin-Konzentration und einer Hemmung der Aktivierung der Mitogen-aktivierten Proteinkinasen ERK1 (p44) und ERK2 (p42). Es verhindert Hypertrophie und Proliferation. Dieses Medikament wird gut vertragen, wobei die häufigsten berichteten Nebenwirkungen Kopfschmerzen, Schwindel und Müdigkeit sind. |
Literatur |
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT04432350 | Withdrawn | COVID|Drug Effect|Drug Interaction|Risk Reduction |
Tabula Rasa HealthCare |
June 12 2020 | -- |
| NCT01570686 | Completed | Hypertension |
Novartis Pharmaceuticals|Novartis |
April 2012 | Phase 4 |
| NCT01519635 | Completed | Hypertension |
Centre Hospitalier Universitaire Vaudois |
October 2011 | Phase 4 |
| NCT01235910 | Terminated | Hypertension|Cardiac Transplantation |
University of Colorado Denver|American Heart Association |
May 2011 | Phase 4 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
