nur für Forschungszwecke
Buspirone HCl 5-HT Receptor Agonist
Kat.-Nr.S4256
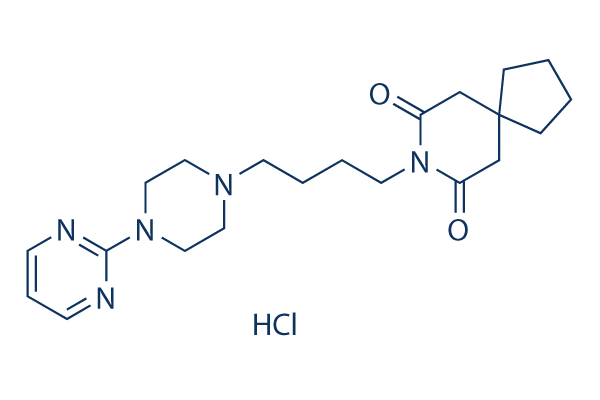
Chemische Struktur
Molekulargewicht: 421.96
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere 5-HT Receptor Inhibitoren | WAY-100635 Maleate Serotonin (5-HT) HCl Puerarin BRL-15572 Dihydrochloride SB269970 HCl Ketanserin RS-127445 Nuciferine Flopropione BRL-54443 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 421.96 | Formel | C21H31N5O2.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 33386-08-2 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | Buspirone hydrochloride | Smiles | C1CCC2(C1)CC(=O)N(C(=O)C2)CCCCN3CCN(CC3)C4=NC=CC=N4.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 84 mg/mL
(199.07 mM)
Water : 84 mg/mL Ethanol : 36 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
5-HT1A
|
|---|---|
| In vitro |
Buspirone, ein klinisch wirksames Nicht-Benzodiazepin-Anxiolytikum, hemmt die Entladung dieser Neuronen, wenn es intravenös (ED50 = 0,011 mg/kg, i.v.), intraperitoneal (ED50 = 0,088 mg/kg, i.p.) und intragastrisch (wirksame Dosis = 1,0-20,0 mg/kg, i.g.) injiziert wird. Buspirone hemmt diese Zellen auch, wenn es durch Mikroiontophorese außerhalb der aufgezeichneten Neuronen verabreicht wird. Buspirone wird hauptsächlich durch oxidativen Metabolismus eliminiert, der mehrere hydroxylierte Metaboliten produziert, einschließlich 5-Hydroxy-Buspirone und 1-Pyrimidinylpiperazin. |
| In vivo |
Buspirone (3 mg/Ratte, i.p.) hemmt dosisabhängig und vollständig die schockinduzierte Ultraschall-Vokalisation nach systemischer Injektion und nach Mikroinjektion in den dorsalen Raphe-Kern von Ratten, einer Gehirnregion, die reich an somatodendritischen 5-HT1A-Rezeptoren ist. Buspirone (20 mg/kg) verringert die Immobilität im Zwangsschwimmtest bei Ratten. Buspirone ist ein serotonerges (5HT(1A) receptor agonist) anxiolytisches Medikament mit einer gewissen D(2) dopaminergen Wirkung in einem Zebrafischmodell für Angstzustände. Buspirone reduziert dosisabhängig LID und verbesserte die l-DOPA-bedingte Motorleistung aufgrund der Wirkung am 5-HT(1A) receptor bei l-DOPA-primären Ratten. Buspirone verzögert die LID-Entwicklung und verbessert gleichzeitig die antiparkinsonische Wirksamkeit von l-DOPA, was auf potenzielle langfristige Vorteile von 5-HT(1A) agonists zur Reduzierung l-DOPA-bedingter Nebenwirkungen bei l-DOPA-naiven Ratten hinweist. |
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05511909 | Recruiting | Opioid Use Disorder|Opioid Withdrawal|Opioid Craving|Anxiety |
Johns Hopkins University |
December 15 2022 | Phase 2 |
| NCT03444831 | Completed | Dyspepsia |
Isfahan University of Medical Sciences |
March 1 2016 | Phase 4 |
| NCT02483598 | Terminated | Gastric Bypass |
North Dakota State University|Neuropsychiatric Research Institute Fargo North Dakota |
June 2015 | Phase 4 |
| NCT01699828 | Completed | Smoking Cessation|Tobacco Use Cessation |
Centre for Addiction and Mental Health |
October 2012 | Phase 1|Phase 2 |
| NCT01496612 | Terminated | Anxiety Disorder|Seizures|Epilepsy|Partial Epilepsy|Depression |
National Institute of Neurological Disorders and Stroke (NINDS)|National Institutes of Health Clinical Center (CC) |
November 22 2011 | Phase 2 |
| NCT00873509 | Completed | Autistic Disorder |
Chugani Diane C.|National Institute of Neurological Disorders and Stroke (NINDS) |
May 2009 | Phase 2|Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
