nur für Forschungszwecke
Ifenprodil Tartrate NMDAR Antagonist
Kat.-Nr.S4091
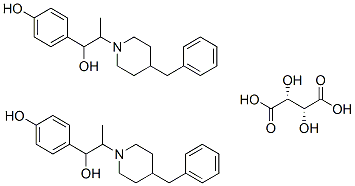
Chemische Struktur
Molekulargewicht: 800.98
Qualitätskontrolle
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 800.98 | Formel | 2(C21H27NO2).C4H6O6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 23210-58-4 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC(C(C1=CC=C(C=C1)O)O)N2CCC(CC2)CC3=CC=CC=C3.CC(C(C1=CC=C(C=C1)O)O)N2CCC(CC2)CC3=CC=CC=C3.C(C(C(=O)O)O)(C(=O)O)O | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(124.84 mM)
Ethanol : 50 mg/mL Water : 8 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
NMDA Receptor
0.3 μM
|
|---|---|
| In vitro |
Ifenprodil hemmt NMDA-induzierte Ströme an NR1A/NR2B- und NR1A/NR2A-Rezeptoren mit einer IC50 von 0,34 μM bzw. 146 μM in Oozyten, die bei -70 mV spannungsfixiert sind. Ifenprodil kann als schwacher Offenkanalblocker von NR1A/NR2A-Rezeptoren wirken; der Grad der Hemmung, der mit 100 μM Ifenprodil an NR1A/NR2A-Rezeptoren beobachtet wird, wird durch Änderungen der extrazellulären Glycinkonzentration nicht verändert. Die hemmende Wirkung von 1 mM Ifenprodil an NR1A/NR2B-Rezeptoren wird durch Erhöhung der Glycinkonzentration reduziert. Ifenprodil (10 μM) hemmt praktisch den gesamten NMDA-Rezeptor-evoziierten Strom in sehr jungen kortikalen Rattenneuronen, die eine einzelne Population von Rezeptoren enthalten, die eine hohe Affinität für Glycin aufweisen. Ifenprodil (10 μM) hemmt sowohl die hochaffine Population als auch einen signifikanten Anteil der niederaffinen Komponente in älteren kortikalen Rattenneuronen, wodurch drei pharmakologisch unterschiedliche Populationen von NMDA-Rezeptoren in einzelnen Neuronen sichtbar werden. Ifenprodil antagonisiert NMDA-Rezeptoren auf aktivitätsabhängige Weise, während es auch die Rezeptoraffinität für Glutamat-Erkennungsstellen-Agonisten erhöht. Ifenprodil-Hemmkurven gegen 10 μM und 100 μM NMDA-evozierte Ströme ergaben IC50-Werte von 0,88 μM bzw. 0,17 μM. Ifenprodil (3 μM) potenziert auf etwa 200 % der Kontrollwerte in kultivierten kortikalen Neuronen von Ratten. Ifenprodil zeigt eine 39- und 50-fach höhere Affinität für die Agonisten-gebundenen aktivierten bzw. desensibilisierten Zustände des NMDA-Rezeptors im Vergleich zum ruhenden, Agonisten-ungebundenen Zustand. Die Ifenprodil-Bindung an den NMDA-Rezeptor führt zu einer 6-fach höheren Affinität für Glutamat-Stellen-Agonisten.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
