nur für Forschungszwecke
NU7026 DNA-PK Inhibitor
Kat.-Nr.S2893
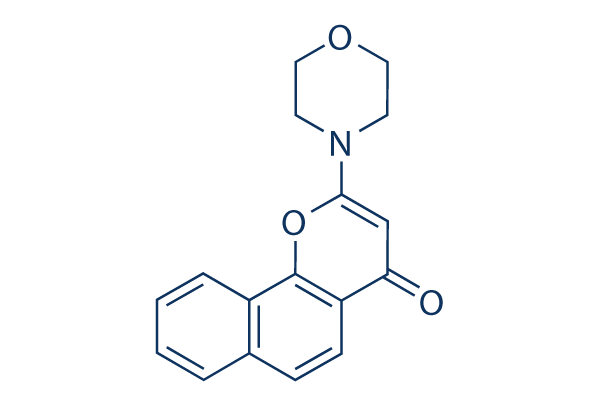
Chemische Struktur
Molekulargewicht: 281.31
Qualitätskontrolle
| Verwandte Ziele | HDAC PARP ATM/ATR WRN DNA/RNA Synthesis Topoisomerase PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere DNA-PK Inhibitoren | Nedisertib (M3814) AZD7648 NU7441 (KU-57788) KU-0060648 VX-984 CC-115 YU238259 LTURM34 Compound 401 |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HeLa cells | Function assay | Inhibition of DNA dependent protein kinase isolated from HeLa cells, IC50=0.23 μM | 15658870 | |||
| HeLa cells | Function assay | Inhibition of mTOR protein isolated from HeLa cells, IC50=6.4 μM | 15658870 | |||
| HeLa | Function assay | In vitro inhibition of DNA-dependent protein kinase(DNA-PK) from HeLa (human carcinoma) cells, IC50=0.23μM | 12941339 | |||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 281.31 | Formel | C17H15NO3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 154447-35-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | LY293646 | Smiles | C1COCCN1C2=CC(=O)C3=C(O2)C4=CC=CC=C4C=C3 | ||
Löslichkeit
|
In vitro |
4-Methylpyridine : 5 mg/mL
DMSO
: 1 mg/mL
(3.55 mM)
Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
DNA-PK
(Cell-free assay) 0.23 μM
PI3K
(Cell-free assay) 13 μM
|
|---|---|
| In vitro |
NU7026 verstärkt die durch ionisierende Strahlung induzierte Zytotoxizität in einer konzentrationsabhängigen Weise in V3YAC- und PARP-1+/+-Zellen. Diese Verbindung hebt die Erholung von potenziell letalen Schäden in wachstumsgehemmten Zellen vollständig auf. Sie hemmt die DNA-DSB-Reparatur um 56 % in der V3YAC-Zelllinie. Diese Chemikalie (10 μM) verstärkt die wachstumshemmenden Wirkungen von Doxorubicin, mAMSA mit PF50-Werten von ungefähr 19 für mAMSA bis ungefähr 2 in K562-Zellen. Sie (10 μM) verstärkt auch die wachstumshemmende Wirkung in dieser Leukämiezelllinie mit einem PF50-Wert von 10,53. Diese Verbindung (10 μM) verstärkt die induzierte G2-Blockade des Zellzyklus in K562-Zellen. Sie verstärkt Topo-II-Gifte, die eine Hemmung der nicht-homologen Endverbindung und einen G2/M-Checkpoint-Arrest beinhalten. Diese Verbindung (10 μM) Exposition von 4 h in Kombination mit 3 Gy Strahlung ist für einen signifikanten radiosensibilisierenden Effekt in CH1 menschlichen Ovarialkarzinomzellen erforderlich. Es (< 10 μM) hat synergistische zytotoxische Aktivität bei nicht-toxischen Dosen dieser Chemikalie in einer CLL-Zelllinie (I83) und in primären CLL-Lymphozyten. Diese Verbindung (10 μM) erhöht den induzierten G(2)/M-Arrest in I83-Zellen. Es (10 μM) verstärkt das induzierte γH2AX während des gesamten Zellzyklus in der I83-Zelllinie. Diese Chemikalie (10 μM) erhöht die induzierte Apoptose in der I83-Zelllinie. Es (55 μM) führt zu einer dramatischen Induktion der Telomerfusion in p53-null MEFs und zu signifikant weniger Telomerfusionen in p53- und Ligase-IV-Doppel-null MEFs. |
| Kinase-Assay |
Rekombinanter Kinase-Assay
|
|
Mammalian DNA-PK (500 ng/μL) wird aus HeLa-Zellkernextrakt nach Chromatographie mittels Q-Sepharose, S-Sepharose und Heparin-Agarose isoliert. Die DNA-PK-Aktivität (250 ng) wird bei 30℃ in einem Endvolumen von 40 μL in einem Puffer gemessen, der 25 mM HEPES (pH 7.4), 12.5 mM MgCl2, 50 mM KCl, 1 mM DTT, 10% v/v Glycerin, 0.1% w/v NP-40 und 1 mg des Substrats GST-p53N66 in Polypropylen-96-Well-Platten enthält. Zu der Assay-Mischung werden verschiedene Konzentrationen dieser Verbindung (in DMSO bei einer Endkonzentration von 1% v/v) hinzugefügt. Nach 10 Minuten Inkubation wird ATP bis zu einer Endkonzentration von 50 μM zusammen mit einem 30-mer doppelsträngigen DNA-Oligonukleotid (Endkonzentration von 0.5 ng/mL) hinzugefügt, um die Reaktion zu initiieren. Nach 1 Stunde Schütteln werden 150 μL PBS zu der Reaktion hinzugefügt und anschließend 5 μL in eine opake weiße 96-Well-Platte überführt, die 45 μL PBS pro Well enthält, wo das GSTp53N66-Substrat für 1 Stunde an die Wells binden kann. Die IC50-Werte für die Verbindungen in allen Enzym-Assays werden aus sigmoidalen Plots unter Verwendung des Grafikpakets Prism abgeleitet, in denen die Enzymaktivität in den variierenden Konzentrationen der Verbindungen gegen die Konzentration der Verbindung aufgetragen wird.
|
|
| In vivo |
NU7026 (20 mg/kg, i.v.) wird bei Mäusen schnell aus dem Plasma eliminiert (0,108/Stunde), was größtenteils auf einen umfangreichen Metabolismus zurückzuführen ist. Die Bioverfügbarkeit nach interperitonealer (i.p.) und p.o. Verabreichung dieser Verbindung in einer Dosis von 20 mg/kg beträgt 20 bzw. 15 %. |
Literatur |
|
Anwendungen
| Methoden | Biomarker | Bilder | PMID |
|---|---|---|---|
| Western blot | pDNA-PKcs S2056 / DNA-PKcs |

|
22131882 |
| Growth inhibition assay | Cell viability |
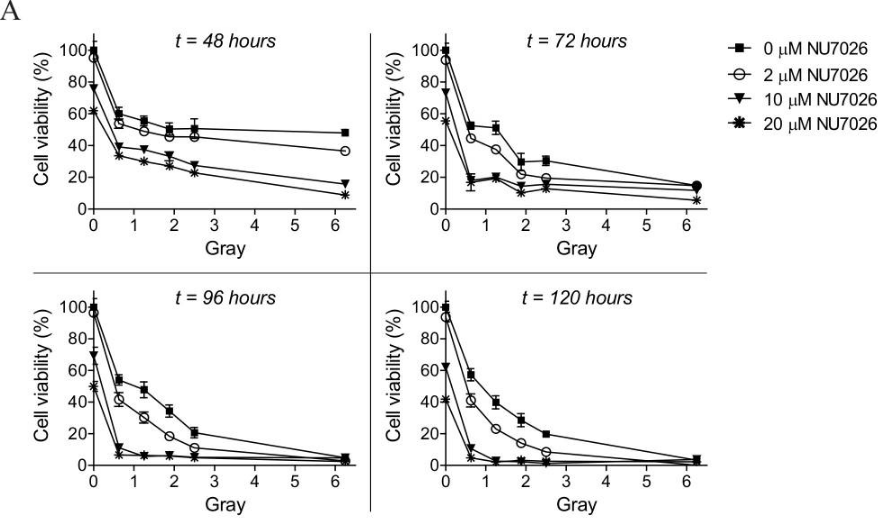
|
26716839 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
