nur für Forschungszwecke
Torcetrapib CETP Inhibitor
Kat.-Nr.S2792
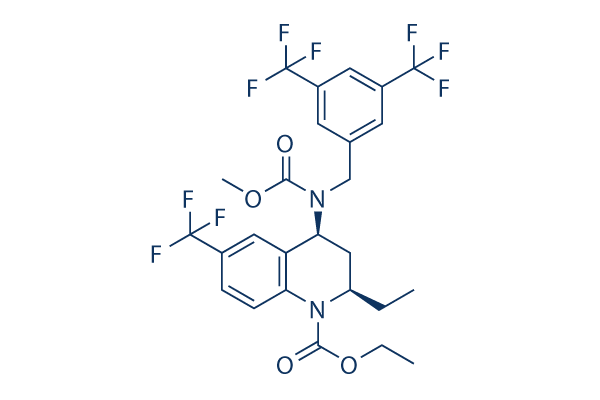
Chemische Struktur
Molekulargewicht: 600.47
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere CETP Inhibitoren | Anacetrapib (MK-0859) Dalcetrapib (JTT-705) Evacetrapib (LY2484595) Obicetrapib |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 600.47 | Formel | C26H25F9N2O4 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 262352-17-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | CP-529414 | Smiles | CCC1CC(C2=C(N1C(=O)OCC)C=CC(=C2)C(F)(F)F)N(CC3=CC(=CC(=C3)C(F)(F)F)C(F)(F)F)C(=O)OC | ||
Löslichkeit
|
In vitro |
DMSO
: 120 mg/mL
(199.84 mM)
Ethanol : 6 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
CETP
37 nM
|
|---|---|
| In vitro |
Torcetrapib erhöht die Aldosteronfreisetzung aus H295R-Zellen dosisabhängig nach entweder 24 oder 48 Stunden Behandlung mit einer EC50 von ungefähr 80 nM. Dieser Effekt wird durch Calciumkanäle vermittelt, da Calciumkanalblocker die durch diese Verbindung induzierte Kortikoidfreisetzung und den Calciumanstieg vollständig blockieren. Diese Chemikalie (1 μM) erhöht signifikant die Expression der steroidogenen Gene CYP11B2 und CYP11B1 in H295R-Zelllinien.
|
| In vivo |
Torcetrapib (< 100 mg, täglich) verändert die Plasmaverteilung von CETP, da das scheinbare Molekulargewicht des CETP nach 2 Stunden nach der Dosis bei gesunden jungen Probanden zu einer größeren Form verschoben ist. Die Behandlung mit dieser Verbindung mit 10 mg, 30 mg, 60 mg und 120 mg täglich sowie 120 mg zweimal täglich führt zu einer Erhöhung des Plasma-HDL-C um 16 %, 28 %, 62 %, 73 % bzw. 91 %, ohne signifikante Veränderungen des TPC bei gesunden jungen Probanden. Es führt zu einem Anstieg des High-Density-Lipoprotein-Cholesterins um 72,1 % und einer Abnahme des Low-Density-Lipoprotein-Cholesterins um 24,9 %, zusätzlich zu einem Anstieg des systolischen Blutdrucks um 5,4 mm Hg, einer Abnahme des Serumkaliums und einem Anstieg von Serumnatrium, Bikarbonat und Aldosteron bei Patienten mit hohem kardiovaskulärem Risiko nach 12-monatiger Behandlung. Dieses Mittel erhöht die HDL-Cholesterinspiegel um 50 % und 60 % bei einer Dosis von 60 mg täglich bzw. 120 mg täglich, sowohl bei gesunden als auch bei moderat hyperlipidämischen Probanden. Es erhöht bei 60 mg täglich den HDL-vermittelten Nettcholesterin-Efflux aus Schaumzellen hauptsächlich durch Erhöhung der HDL-Konzentrationen, während 120 mg täglich dieser Verbindung den Cholesterin-Efflux sowohl durch Erhöhung der HDL-Konzentration als auch durch einen erhöhten Efflux bei angepassten HDL-Konzentrationen erhöht. Diese Chemikalie (90 mg/kg/Tag) führt zu einer 70%igen Hemmung des CE-Transfers bei Kaninchen, die mit einer atherogenen Diät gefüttert wurden. Es (90 mg/kg/Tag) erhöht die mittleren HDL-C-Spiegel um mehr als das 3-fache und die apoA-I-Spiegel um das 2,5-fache im Plasma bei Kaninchen, die mit einer atherogenen Diät gefüttert wurden. Das behandelte Tier weist einen mehrfachen Anstieg der HDL-C-AUC und eine entsprechende Reduktion der Aortenläsionsfläche mit einer 60%igen Reduktion des freien Cholesterins (FC) und Cholesterylesters (EC) in der Aorta bei Kaninchen auf, die mit einer atherogenen Diät gefüttert wurden. Sera von mit dieser Verbindung behandelten Kaninchen stimulieren den freien Cholesterin-Efflux in einem signifikant größerem Maße als Sera von Kontrollkaninchen.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00139061 | Completed | Hyperlipidemia |
Pfizer |
March 2005 | Phase 3 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
