nur für Forschungszwecke
Anacetrapib (MK-0859) CETP Inhibitor
Kat.-Nr.S2748
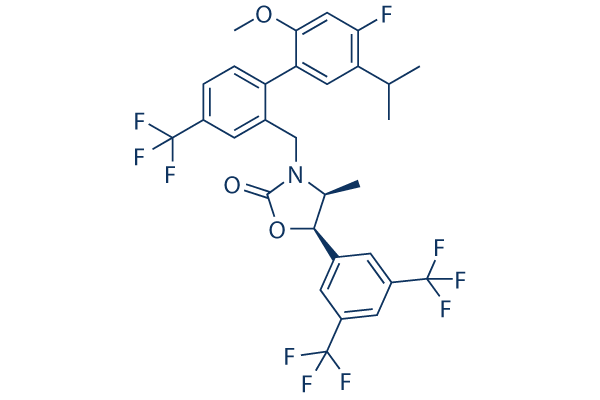
Chemische Struktur
Molekulargewicht: 637.51
Qualitätskontrolle
| Verwandte Ziele | Dehydrogenase HSP Transferase P450 (e.g. CYP17) PDE phosphatase PPAR Vitamin Carbohydrate Metabolism Mitochondrial Metabolism |
|---|---|
| Weitere CETP Inhibitoren | Dalcetrapib (JTT-705) Torcetrapib Evacetrapib (LY2484595) Obicetrapib |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 637.51 | Formel | C30H25F10NO3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 875446-37-0 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1C(OC(=O)N1CC2=C(C=CC(=C2)C(F)(F)F)C3=CC(=C(C=C3OC)F)C(C)C)C4=CC(=CC(=C4)C(F)(F)F)C(F)(F)F | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(156.86 mM)
Ethanol : 100 mg/mL Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
rhCETP
7.9 nM
Mutant CETP (C13S)
11.8 nM
|
|---|---|
| In vitro |
Anacetrapib (MK-0859) ist nicht nur in der Lage, das HDL-Cholesterin zu erhöhen, sondern senkt auch das LDL-Cholesterin weiter, wenn es in Kombination mit einem Statin eingenommen wird. Es verringert dosisabhängig und signifikant die Übertragung von CE von HDL3 auf HDL2. Diese Verbindung beeinflusst nicht die Menge an [14C]-Dalcetrapibthiol, das an rhCETP gebunden ist. Es reduziert die prä-β-HDL-Bildung um mehr als 46 %. Anacetrapib blockiert wirksam die CE- und TG-Übertragung in 95 % menschlichem Serum.
|
| In vivo |
In einem dyslipidämischen Hamstermodell führt 60 mg/kg/Tag Anacetrapib (MK-0859) über 2 Wochen zu einer Reduktion der CETP-Aktivität um 94 % und einem Anstieg des HDL-Cholesterins um 47 % im Vergleich zu Kontrolltieren; die Non-HDL-Cholesterin-Konzentrationen sind nicht betroffen. Diese Verbindung fördert auch den reversen Cholesterintransport aus Makrophagen und führt zu einem Anstieg des fäkalen Cholesteringehalts um 30 %. HDL von behandelten Hamstern zeigt einen Anstieg des SR-B1- und ABCG1-vermittelten Efflux im Vergleich zu Kontrollen. Nach oraler Verabreichung von [14C]Anacetrapib bei 10 mg/kg werden über 48 Stunden nach der Dosis bei Ratten und Affen jeweils ∼80 und 90 % der radioaktiven Dosis wiedergefunden. Der Großteil der verabreichten radioaktiven Dosis wird bei beiden Spezies unverändert im Kot ausgeschieden.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT01122667 | Completed | Dyslipidemia |
Merck Sharp & Dohme LLC |
June 2010 | Phase 1 |
| NCT01114490 | Completed | Dyslipidemia |
Merck Sharp & Dohme LLC |
May 2010 | Phase 1 |
| NCT00325455 | Terminated | Hypercholesterolemia|Mixed Hyperlipemia |
Merck Sharp & Dohme LLC |
June 2006 | Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
