nur für Forschungszwecke
Irinotecan (CPT-11) Topoisomerase I Inhibitor
Kat.-Nr.S1198
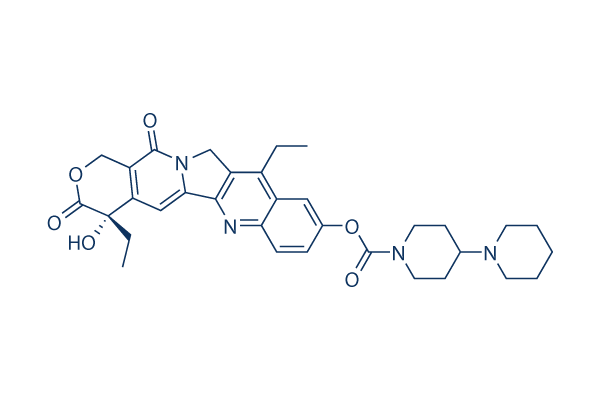
Chemische Struktur
Molekulargewicht: 586.68
Qualitätskontrolle
| Verwandte Ziele | HDAC PARP ATM/ATR DNA-PK WRN DNA/RNA Synthesis PPAR Sirtuin Casein Kinase eIF |
|---|---|
| Weitere Topoisomerase Inhibitoren | Camptothecin (CPT) Betulinic acid Beta-Lapachone (S)-10-Hydroxycamptothecin Amonafide Voreloxin (SNS-595) hydrochloride Ellagic acid Cu(II)-Elesclomol Hydroxy Camptothecine Rubitecan |
Zellkultur, Behandlung & Arbeitskonzentration
| Zelllinien | Assay-Typ | Konzentration | Inkubationszeit | Formulierung | Aktivitätsbeschreibung | PMID |
|---|---|---|---|---|---|---|
| HCT116 | cytotoxicity assay | 10 μM | DMSO | ID50=540 nM | ||
| VM46 | cytotoxicity assay | 10 μM | DMSO | ID50=220 nM | ||
| MCF-7ADR | cytotoxicity assay | 10 μM | DMSO | ID50>500 nM | ||
| L1210 | cytotoxicity assay | IC50=1.2 µM | ||||
| RPMI8402 | cytotoxicity assay | 100 μM | IC50=570 nM | |||
| A-549 | cytotoxicity assay | ~20 μM | DMSO | IC50=6.528 μM | ||
| LOVO | cytotoxicity assay | ~20 μM | DMSO | IC50=9.015 μM | ||
| MCF7 | cytotoxicity assay | ~20 μM | DMSO | IC50=17.403 μM | ||
| LS174T | Growth inhibitory assay | DMSO | IC50=1.16 μM | |||
| KB3-1 | cytotoxicity assay | IC50=0.68 μM | ||||
| KBV-1 | cytotoxicity assay | IC50=40 μM | ||||
| KBH5.0 | cytotoxicity assay | IC50=7.4 μM | ||||
| Hep G2 | Growth inhibitory assay | ~10 μM | DMSO | IC50=5.94 μM | ||
| Hep 3B | Growth inhibitory assay | ~10 μM | DMSO | IC50=4.73 μM | ||
| Hep 2.2. | Growth inhibitory assay | ~10 μM | DMSO | IC50>10 μM | ||
| A549 | cytotoxicity assay | DMSO | IC50=4.61 μM | |||
| MDA-MB-435 | cytotoxicity assay | DMSO | IC50=1.14 μM | |||
| LOVO | cytotoxicity assay | DMSO | IC50=4.99 μM | |||
| MDA-MB-435 | cytotoxicity assay | DMSO | IC50=17 μM | |||
| NCI60 | Growth inhibitory assay | DMSO | GI50=14.1254 μM | |||
| H460 | cytotoxicity assay | DMSO | IC50=0.015 μM | |||
| PC-3 | cytotoxicity assay | DMSO | IC50=0.22 μM | |||
| HT29 | cytotoxicity assay | DMSO | IC50=0.004 μM | |||
| SK-MEL-2 | cytotoxicity assay | DMSO | IC50=0.1 μM | |||
| A375 | cytotoxicity assay | DMSO | IC50=0.004 μM | |||
| Malme-3M | cytotoxicity assay | DMSO | IC50=0.2 μM | |||
| DU 145 | cytotoxicity assay | DMSO | IC50=0.2 μM | |||
| LNCaP | cytotoxicity assay | DMSO | IC50=0.009 μM | |||
| IGROV-1 | cytotoxicity assay | DMSO | IC50=0.03 μM | |||
| KB | cytotoxicity assay | ~20 μM | DMSO | IC50=9.83 μM | ||
| KB-vin | cytotoxicity assay | ~20 μM | DMSO | IC50>20 μM | ||
| Klicken Sie hier, um weitere experimentelle Daten zu Zelllinien anzuzeigen | ||||||
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 586.68 | Formel | C33H38N4O6 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 97682-44-5 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | (+)-Irinotecan,CPT-11 | Smiles | CCC1=C2CN3C(=CC4=C(C3=O)COC(=O)C4(CC)O)C2=NC5=C1C=C(C=C5)OC(=O)N6CCC(CC6)N7CCCCC7 | ||
Löslichkeit
|
In vitro |
DMSO
: 25 mg/mL
(42.61 mM)
Water : Insoluble Ethanol : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Merkmale |
Irinotecan is a prodrug that is used to treat metastatic colorectal cancer.
|
|---|---|
| Targets/IC50/Ki |
Topo I
(LoVo, HT-29 cells) |
| In vitro |
Irinotecan wird durch Carboxylesterasen zu SN-38 aktiviert, um mit seinem Target, Topoisomerase I, interagieren zu können. Diese Verbindung induziert bei ihrer IC50 in LoVo-Zellen und HT-29-Zelllinien ähnliche Mengen an spaltbaren Komplexen. SN-38 induziert eine konzentrationsabhängige Bildung von spaltbaren Komplexen, die sich in LoVo-Zellen und HT-29-Zelllinien nicht signifikant unterscheidet. Die Zellakkumulation dieser Chemikalie ist deutlich unterschiedlich und erreicht in HT-29-Zellen stets höhere Werte als in LoVo-Zellen. Der Lacton-E-Ring dieser Verbindung und SN-38 hydrolysiert reversibel in wässrigen Lösungen, und die Umwandlung zwischen den Lacton- und Carboxylatformen ist pH- und temperaturabhängig. Die Leber ist hauptsächlich für die Aktivierung dieses Wirkstoffs zu SN-38 verantwortlich. Bei gleichen Konzentrationen dieses Medikaments und SN-38-Glucuronid ist die Rate der Beta-Glucuronidase-vermittelten SN-38-Produktion höher als die, die aus dieser Verbindung in sowohl Tumor- als auch Normalgewebe gebildet wird. Es wird auch in Darm, Plasma und Tumorgeweben zu SN-38 umgewandelt. Dieser Wirkstoff ist in SCLC-Zelllinien signifikant aktiver als in NSCLC-Zelllinien, während bei SN-38 kein signifikanter Unterschied zwischen histologischen Typen beobachtet wird.
|
| In vivo |
In COLO 320 Xenografts induziert Irinotecan eine maximale Wachstumshemmung von 92 %. Eine Einzeldosis dieser Verbindung erhöht signifikant die Mengen an Topoisomerase I, die kovalent an die DNA im Magen, Zwölffingerdarm, Dickdarm und der Leber gebunden sind. Gleichzeitig zeigt die mit Irinotecan behandelte Gruppe signifikant höhere Mengen an DNA-Strangbrüchen in Kolonschleimhautzellen im Vergleich zur Kontrollgruppe.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT05854498 | Recruiting | Metastatic Colorectal Cancer |
University of Wisconsin Madison|Ipsen |
October 13 2023 | Phase 2 |
| NCT05732129 | Not yet recruiting | Homologous Recombination Deficiency Alterations Metastatic Colorectal Cancer |
Fudan University |
March 1 2023 | Phase 2 |
| NCT05731518 | Recruiting | Small Cell Lung Cancer |
Biocity Biopharmaceutics Co. Ltd. |
February 23 2023 | Phase 1|Phase 2 |
| NCT06003998 | Recruiting | Colorectal Cancer|Peritoneal Metastases |
Catharina Ziekenhuis Eindhoven |
December 27 2022 | Phase 2 |
| NCT05277766 | Recruiting | Peritoneal Carcinomatosis|Peritoneal Metastases|Colorectal Cancer|Small Bowel Cancer|Appendix Cancer|Gastric Cancer|Pancreatic Cancer|Bile Duct Cancer |
University Hospital Ghent|Kom Op Tegen Kanker|University Ghent |
November 21 2022 | Phase 1 |
| NCT05379790 | Recruiting | Gastric Cancer|Peritoneal Metastases |
Erasmus Medical Center |
May 25 2022 | Phase 1 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
