nur für Forschungszwecke
SB743921 HCl Kinesin Inhibitor
Kat.-Nr.S2182
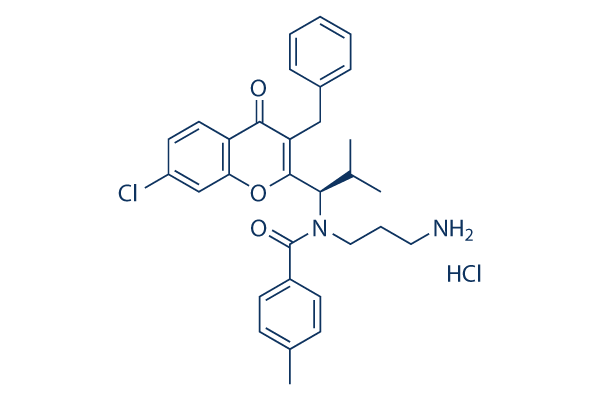
Chemische Struktur
Molekulargewicht: 553.52
Qualitätskontrolle
| Verwandte Ziele | Akt Wnt/beta-catenin PKC HSP ROCK Microtubule Associated Integrin Bcr-Abl Actin FAK |
|---|---|
| Weitere Kinesin Inhibitoren | GSK923295 Ispinesib (SB-715992) Monastrol ARQ 621 K 858 BTB-1 VLS-1488(KIF18A-IN-6 ) H-Cys(Trt)-OH Filanesib hydrochloride GW406108X |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 553.52 | Formel | C31H33N2O3.HCl |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 940929-33-9 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | N/A | Smiles | CC1=CC=C(C=C1)C(=O)N(CCCN)C(C2=C(C(=O)C3=C(O2)C=C(C=C3)Cl)CC4=CC=CC=C4)C(C)C.Cl | ||
Löslichkeit
|
In vitro |
DMSO
: 100 mg/mL
(180.66 mM)
Ethanol : 100 mg/mL Water : 46 mg/mL |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
KSP (MX1 cells)
0.06 nM
KSP (Colo205 cells)
0.07 nM
KSP
0.1 nM(Ki)
KSP (SKOV3 cells)
0.2 nM
KSP (MV522 cells)
1.7 nM
KSP (P388 cells)
14.4 nM
|
|---|---|
| In vitro |
Der Ki von SB 743921 für menschliches und Maus-KSP beträgt 0,1 nM bzw. 0,12 nM, während der Ki von SB 743921 für andere Kinesin, einschließlich MKLP1, Kin2, mehr als 70 μM beträgt. SB 743921 blockiert die Bildung einer funktionellen mitotischen Spindel, wodurch es zu einem Zellzyklusarrest in der Mitose und anschließendem Zelltod kommt. SB-743921 hat eine verbesserte Wirksamkeit gegenüber Ispinesib sowohl in biochemischen als auch in zellulären Assays.
|
| Kinase-Assay |
Biochemie-Assay
|
|
Die Motordomänen von KSP (Aminosäuren 1–360) werden in Escherichia coli BL21(DE3) als COOH-terminale 6-His-Fusionsproteine exprimiert. Bakterienzellen werden in einem Mikrofluidizer mit einem Lysepuffer [50 mM Tris-HCl; 50 mM KCl, 10 mM Imidazol, 2 mM MgCl2, 8 mM β-Mercaptoethanol, 0,1 mM ATP (pH 7,4)] lysiert, und Proteine werden mittels Ni-NTA-Agarose-Affinitätschromatographie gereinigt, mit einem Elutionspuffer bestehend aus 50 mM PIPES, 10 % Saccharose, 300 mM Imidazol, 50 mM KCl, 2 mM MgCl2, mM β-Mercaptoethanol und 0,1 mM ATP (pH 6,8). Steady-State-Messungen der ATPase-Aktivität werden mit einem Pyruvatkinase-Lactatdehydrogenase-Detektionssystem durchgeführt, das das Auftreten von ADP mit der Oxidation von NADH koppelt. Absorptionsänderungen werden bei 340 nm überwacht. Alle biochemischen Experimente werden in PEM25-Puffer [25 mM Pipes/KOH (pH 6,8), 2 mM MgCl2, 1 mM EGTA] durchgeführt, ergänzt mit 10 μM SB 743921 für Experimente, die Mikrotubuli beinhalten. Die Raten der ADP-Freisetzung werden in einem Stopped-Flow-Apparat gemessen; die Abnahme der Fluoreszenz von MANT-ATP wird überwacht. Die Raten der Pi-Freisetzung werden in einem Stopped-Flow-Apparat gemessen, unter Verwendung von bakteriellem Phosphat-bindendem Protein, das mit 7-Diethylamino-3-((((2 maleimidyl)ethyl)amino)carbonyl)coumarin (MDCC)-Farbstoff modifiziert ist. Ki-Schätzungen von KSP-Inhibitoren werden aus den Dosis-Wirkungs-Kurven extrahiert, mit expliziter Korrektur für die Enzymkonzentration. Die Tubulin-Polymerisation wird durch Messung von Absorptionsänderungen bei 340 nm überwacht. Der Assay wird in 100-μL-Volumen in 96-Well-Halbflächen-Mikrotiterplatten unter Verwendung eines Mikroplattenlesers bei einer Inkubationstemperatur von 37 °C durchgeführt.
|
|
| In vivo |
SB-743921 zeigt in vivo eine höhere Wirksamkeit gegen P388-Leukämie. SB-743921 hat eine signifikante Wirksamkeit in einem breiten Spektrum von Tumormodellen, die sich von denen der Taxane unterscheiden. Es wurde gezeigt, dass SB-743921 Aktivität gegen fortgeschrittene menschliche Tumor-Xenografts Colo205 (vollständige Regressionen), MCF-7, SK-MES, H69, OVCAR-3 (vollständige und partielle Regressionen) und HT-29, MX-1, MDA-MB-231, A2780 (Tumorwachstumsverzögerung) aufweist. SB-743921 verursacht nicht die Neuropathie, die oft mit den Tubulin-Wirkstoffen verbunden ist.
|
Literatur |
|
Klinische Studieninformationen
(Daten von https://clinicaltrials.gov, aktualisiert am 2024-05-22)
| NCT-Nummer | Rekrutierung | Erkrankungen | Sponsor/Kooperationspartner | Startdatum | Phasen |
|---|---|---|---|---|---|
| NCT00343564 | Completed | Non-Hodgkin''s Lymphoma|Hodgkin''s Disease |
Cytokinetics |
April 2006 | Phase 1|Phase 2 |
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
