nur für Forschungszwecke
Blonanserin 5-HT Receptor Antagonist
Kat.-Nr.S2112
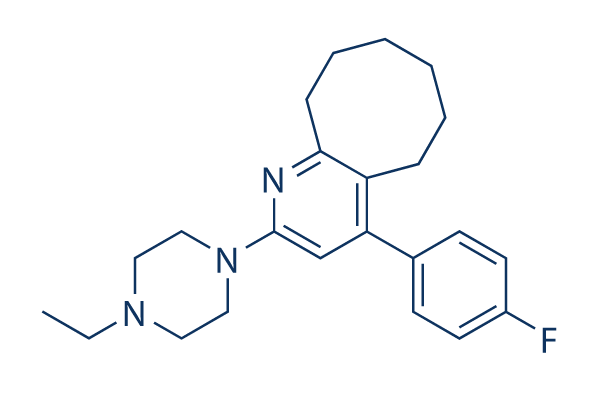
Chemische Struktur
Molekulargewicht: 367.5
Qualitätskontrolle
- In Nature Medicine für seine erstklassige Qualität zitiert
- COA
- NMR
- HPLC
- SDS
- Datenblatt
| Verwandte Ziele | Adrenergic Receptor AChR COX Calcium Channel Histamine Receptor Dopamine Receptor GABA Receptor TRP Channel Cholinesterase (ChE) GluR |
|---|---|
| Weitere 5-HT Receptor Inhibitoren | WAY-100635 Maleate Serotonin (5-HT) HCl Puerarin BRL-15572 Dihydrochloride SB269970 HCl Ketanserin RS-127445 Nuciferine Flopropione BRL-54443 |
Chemische Informationen, Lagerung & Stabilität
| Molekulargewicht | 367.5 | Formel | C23H30FN3 |
Lagerung (Ab dem Eingangsdatum) | |
|---|---|---|---|---|---|
| CAS-Nr. | 132810-10-7 | SDF herunterladen | Lagerung von Stammlösungen |
|
|
| Synonyme | AD 5423 | Smiles | CCN1CCN(CC1)C2=NC3=C(CCCCCC3)C(=C2)C4=CC=C(C=C4)F | ||
Löslichkeit
|
In vitro |
5%TFA : 3 mg/mL
DMSO
: Insoluble
Water : Insoluble |
Molaritätsrechner
|
In vivo |
|||||
In-vivo-Formulierungsrechner (Klare Lösung)
Schritt 1: Geben Sie die untenstehenden Informationen ein (Empfohlen: Ein zusätzliches Tier zur Berücksichtigung von Verlusten während des Experiments)
Schritt 2: Geben Sie die In-vivo-Formulierung ein (Dies ist nur der Rechner, keine Formulierung. Bitte kontaktieren Sie uns zuerst, wenn es im Abschnitt "Löslichkeit" keine In-vivo-Formulierung gibt.)
Berechnungsergebnisse:
Arbeitskonzentration: mg/ml;
Methode zur Herstellung der DMSO-Stammlösung: mg Wirkstoff vorgelöst in μL DMSO ( Konzentration der Stammlösung mg/mL, Bitte kontaktieren Sie uns zuerst, wenn die Konzentration die DMSO-Löslichkeit der Wirkstoffcharge überschreitet. )
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügenμL PEG300, mischen und klären, dann hinzufügenμL Tween 80, mischen und klären, dann hinzufügen μL ddH2O, mischen und klären.
Methode zur Herstellung der In-vivo-Formulierung: Nehmen Sie μL DMSO Stammlösung, dann hinzufügen μL Maisöl, mischen und klären.
Hinweis: 1. Bitte stellen Sie sicher, dass die Flüssigkeit klar ist, bevor Sie das nächste Lösungsmittel hinzufügen.
2. Achten Sie darauf, das/die Lösungsmittel der Reihe nach hinzuzufügen. Sie müssen sicherstellen, dass die bei der vorherigen Zugabe erhaltene Lösung eine klare Lösung ist, bevor Sie mit der Zugabe des nächsten Lösungsmittels fortfahren. Physikalische Methoden wie Vortex, Ultraschall oder ein heißes Wasserbad können zur Unterstützung des Lösens verwendet werden.
Wirkmechanismus
| Targets/IC50/Ki |
5-HT2
3.98 nM(Ki)
dopamine D2 receptor
14.8 nM(Ki)
|
|---|---|
| In vitro |
Blonanserin erhöht vorübergehend die neuronale Aktivität im Locus coeruleus und in der ventralen tegmentalen Area, aber nicht im dorsalen Raphe-Kern oder im mediodorsalen Thalamuskern, während Risperidon die Aktivität im Locus coeruleus, in der ventralen tegmentalen Area und im dorsalen Raphe-Kern, aber nicht im mediodorsalen Thalamuskern von Ratten erhöht. Diese Verbindung erhöht anhaltend die extrazellulären frontal gelegenen Spiegel von Noradrenalin und Dopamin, aber nicht Serotonin, GABA oder Glutamat, während Risperidon anhaltend die Spiegel von Noradrenalin, Dopamin und Serotonin, aber nicht GABA oder Glutamat erhöht. Es erhöht den Ausstrom von kortikalem DA und seinen Metaboliten, Homovanillinsäure und 3,4-Dihydroxyphenylessigsäure. Diese Chemikalie zeigt die potenteste Bindungsaffinität für menschliche D3-Rezeptoren unter den getesteten atypischen Antipsychotika (Risperidon, Olanzapin und Aripiprazol). Es wirkt als potenter vollständiger Antagonist für menschliche D3-Rezeptoren. Es blockiert die Bindung von [(3)H]-(+)-PHNO, einem D2/D3-Rezeptor-Radiotracer, sowohl in der D2-Rezeptor-reichen Region (Striatum) als auch in der D3-Rezeptor-reichen Region (Kleinhirn-Lappen 9 und 10). Dieser Wirkstoff, ein neuartiges atypisches Antipsychotikum mit dopamin-D(2)/Serotonin-5-HT(2A)-antagonistischen Eigenschaften, zeigt eine gute Hirnverteilung.
|
| In vivo |
Blonanserin, 1 mg/kg, aber nicht 0,3 mg/kg, verbessert das PCP-induzierte NOR-Defizit bei Ratten. Diese Verbindung kehrt das NOR-Defizit signifikant um, ohne die Aktivität während der Erwerbs- oder Retentionsphasen bei Ratten zu verringern.
|
Literatur |
|
Technischer Support
Tel: +1-832-582-8158 Ext:3
Wenn Sie weitere Fragen haben, hinterlassen Sie bitte eine Nachricht.
